ائوزینوفیلی - ویکیپدیا، دانشنامهٔ آزاد
| ائوزینوفیلی | |
|---|---|
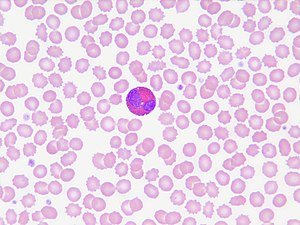 | |
| ائوزینوفیلها در خون محیطی بیماری که به ائوزینوفیلی ایدیوپاتیک دچار است | |
| تخصص | بیماری عفونی، خونشناسی |
| طبقهبندی و منابع بیرونی | |
| پیشنت پلاس | ائوزینوفیلی |
ائوزینوفیلی (انگلیسی: Eosinophilia) وضعیتی است که در آن شمار ائوزینوفیلها در خون محیطی از ۵×۱۰۸/L (۵۰۰/μL) فراتر رود. هایپرائوزینوفیلی افزایش شمار ائوزینوفیلهای خون در گردش افراد به بالای ۱٫۵×۱۰۹/L (یعنی ۱۵۰۰/μL) است. سندرم هیپرائوزینوفیلیک افزایش پایدار در این تعداد بالای ۱٫۵×۱۰۹/L (یعنی ۱۵۰۰/μL) است که با شواهد آسیب بافتی مبتنی بر ائوزینوفیل نیز همراه است.[۱]
ائوزینوفیلها معمولاً کمتر از ۷ درصد لکوسیتهای در گردش را تشکیل میدهند. افزایش قابل توجهی در شمار ائوزینوفیلهای بافت غیر خونی که در معاینه هیستوپاتولوژیک مشاهده میشود، برای ائوزینوفیلی بافتی تشخیصی است. چندین علت شناخته شدهاست که شایعترین آنها نوعی واکنش آلرژیک یا عفونت انگلی است. تشخیص ائوزینوفیلی از طریق شمارش کامل خون (CBC) انجام میشود، اما روشهای تشخیصی که بر اساس علت زمینهای انجام میشوند بسته به شرایط مشکوک متفاوت است. اگر CBC ائوزینوفیلی مشخص را نشان دهد، بهطور کلی نیازی به شمارش ائوزینوفیل مطلق نیست. محل عامل علت را میتوان برای طبقهبندی ائوزینوفیلی به دو نوع کلی استفاده کرد: بیرونی، که در آن عامل خارج از عوامل سلولی ائوزینوفیل قرار دارد. و ائوزینوفیلی درونی، که نشان دهنده علل درون رده سلولی ائوزینیفیل است. درمانهای خاص بر اساس شرایط ایجادکننده تعیین میشوند، اگرچه در ائوزینوفیلی ایدیوپاتیک، بیماری ممکن است با کورتیکواستروئیدها کنترل شود.[۲] ائوزینوفیلی یک اختلال نیست (بلکه تنها یک علامت) مگر اینکه ایدیوپاتیک باشد.
بهطور غیررسمی، سطح ائوزینوفیل خون اغلب به صورت خفیف در شمارش ۵۰۰–۱۵۰۰/μL بالا، متوسط میان ۱۵۰۰–۵۰۰۰/μL افزایش یافته و زمانی که بیش از ۵۰۰۰/μL باشد به شدت افزایش مییابد. افزایش شمار ائوزینوفیل خون میتواند گذرا، پایدار، مکرر یا دورهای باشد.[۳][۴]
شمار ائوزینوفیلها در خون انسان بهطور معمول میان ۱۰۰ تا ۵۰۰ در هر میکرولیتر است. حفظ این سطوح ناشی از تعادل میان تولید ائوزینوفیلها توسط سلولهای پیشساز ائوزینوفیل مغز استخوان به نام CFU-Eos و مهاجرت ائوزینوفیلهای در گردش به خارج از خون از راه ونولهای پسمویرگی به بافتها است. ائوزینوفیلها درصد کمی از لکوسیتهای خون محیطی (معمولاً کمتر از ۸ درصد) را نشان میدهند، نیمه عمری در گردش خون تنها ۸ تا ۱۸ ساعت دارند، اما حداقل برای چندین هفته در بافتها باقی میمانند.[۵][۶]
ائوزینوفیلها یکی از اشکال گرانولوسیتهای تمایز نهایی هستند. آنها برای خنثی کردن میکروبهای مهاجم، عمدتاً انگلها و کرمها، و همچنین انواع خاصی از قارچها و ویروسها عمل میکنند. آنها همچنین در رد پیوند، بیماری پیوند در مقابل میزبان و کشتن سلولهای تومور شرکت میکنند. در انجام این عملکردها، ائوزینوفیلها طیفی از گونههای اکسیژن فعال سمی (مانند هیپوبرومیت، اسید هیپوبرومو، سوپراکسید و پراکسید) را تولید و آزاد میکنند و همچنین در صورت نیاز یک آرمنتاریوم از پیش ساختهشده از سیتوکینها، کموکینها، عوامل واسطهای رشد آزاد میکنند. به عنوان مثال، لوکوترینها، پروستاگلاندینها، فاکتور فعال کننده پلاکت) و پروتئینهای سمی (مثلاً متالوپروتئینازها، پروتئین اساسی اصلی، پروتئین کاتیونی ائوزینوفیل، ائوزینوفیل پراکسیداز، و نوروتوکسین مشتق از ائوزینوفیل). این عوامل برای تنظیم پاسخهای ایمنی قوی و التهابی که میکروبهای مهاجم، بافت خارجی و سلولهای بدخیم را از بین میبرند، عمل میکنند. هنگامی که ائوزینوفیلها بیش از حد تولید و بیش از حد فعال میشوند، که در موارد خاصی از هیپرائوزینوفیلی و تا حدی ائوزینوفیلی رخ میدهد، ممکن است گونههای اکسیژن فعال و مولکولهای از پیش ساخته شده خود را به سمت بافتهای طبیعی هدایت کنند. این مورد میتواند منجر به آسیب جدی به اندامهایی مانند ریه، قلب، کلیهها و مغز شود.[۶][۷][۸]
منابع[ویرایش]
- ↑ "Eosinophilic Disorders". Merck & Co. Retrieved 2012-11-02.
- ↑ Beers, Mark; Porter, Robert; Jones, Thomas (2006). "Ch. 11". The Merck Manual of Diagnosis and Therapy (18th ed.). Whitehouse Station, New Jersey: Merck Research Laboratories. pp. 1093–6. ISBN 0-911910-18-2.
- ↑ Butt NM, Lambert J, Ali S, Beer PA, Cross NC, Duncombe A, Ewing J, Harrison CN, Knapper S, McLornan D, Mead AJ, Radia D, Bain BJ (2017). "Guideline for the investigation and management of eosinophilia" (PDF). British Journal of Haematology. 176 (4): 553–572. doi:10.1111/bjh.14488. PMID 28112388.
- ↑ Gotlib J (2017). "World Health Organization-defined eosinophilic disorders: 2017 update on diagnosis, risk stratification, and management". American Journal of Hematology. 92 (11): 1243–1259. doi:10.1002/ajh.24880. PMID 29044676.
- ↑ Beeken WL, Northwood I, Beliveau C, Baigent G, Gump D (1987). "Eosinophils of human colonic mucosa: C3b and Fc gamma receptor expression and phagocytic capabilities". Clinical Immunology and Immunopathology. 43 (3): 289–300. doi:10.1016/0090-1229(87)90138-3. PMID 2953511.
- ↑ ۶٫۰ ۶٫۱ Kovalszki A, Weller PF (2016). "Eosinophilia". Primary Care. 43 (4): 607–617. doi:10.1016/j.pop.2016.07.010. PMC 5293177. PMID 27866580.
- ↑ Roufosse F (2013). "L4. Eosinophils: how they contribute to endothelial damage and dysfunction". Presse Médicale. 42 (4 Pt 2): 503–7. doi:10.1016/j.lpm.2013.01.005. PMID 23453213.
- ↑ Long H, Liao W, Wang L, Lu Q (2016). "A Player and Coordinator: The Versatile Roles of Eosinophils in the Immune System". Transfusion Medicine and Hemotherapy. 43 (2): 96–108. doi:10.1159/000445215. PMC 4872051. PMID 27226792.
پیوند به بیرون[ویرایش]
| در ویکیانبار پروندههایی دربارهٔ ائوزینوفیلی موجود است. |


 French
French Deutsch
Deutsch