نیتروز اکسید - ویکیپدیا، دانشنامهٔ آزاد
| نیتروز اکسید | |
|---|---|
 | |
 | |
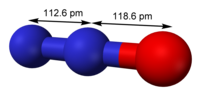
Dinitrogen monoxide | |
دیگر نامها Laughing gas sweet air | |
| شناساگرها | |
| شماره ثبت سیایاس | ۱۰۰۲۴-۹۷-۲ |
| پابکم | ۹۴۸ |
| کماسپایدر | ۹۲۳ |
| UNII | K50XQU1029 |
| شمارهٔ یواِن | 1070 (compressed) 2201 (liquid) |
| KEGG | D00102 |
| ChEBI | CHEBI:17045 |
| ChEMBL | CHEMBL۳۳۵۹۰۰ |
| شمارهٔ آرتیئیسیاس | QX1350000 |
| کد اِیتیسی | N01 |
| جیمول-تصاویر سه بعدی | Image 1 |
| |
| |
| خصوصیات | |
| فرمول مولکولی | N2O |
| جرم مولی | 44.013 g/mol |
| شکل ظاهری | colorless gas |
| چگالی | 1.977 g/L (gas) |
| دمای ذوب | −۹۰٫۸۶ °C (182.29 K) |
| دمای جوش | −۸۸٫۴۸ °C (184.67 K) |
| انحلالپذیری در آب | 0.15 g/100 ml (15 °C) |
| انحلالپذیری | soluble in الکل، اتر، سولفوریک اسید |
| log P | 0.35 |
| فشار بخار | 5150 kPa (20 °C) |
| ضریب شکست (nD) | 1.330 |
| ساختار | |
| شکل مولکولی | linear C∞v |
| گشتاور دوقطبی | 0.166 D |
| ترموشیمی | |
آنتروپی مولار استاندارد S | 219.96 J K-1 mol-1 |
آنتالپی استاندارد تشکیل ΔfH | +82.05 kJ/mol |
| داروشناسی | |
| Routes of administration | دم (تنفس) |
| دگرگشت | 0.004% |
| Elimination half-life | 5 minutes |
| دفع | دستگاه تنفسی |
| ردهبندی داروهای بارداری | |
| خطرات | |
| MSDS | Ilo.org, ICSC 0067 |
| شاخص ئییو | Oxidant [O] |
| لوزی آتش | |
| نقطه اشتعال | |
| ترکیبات مرتبط | |
| مرتبط با نیتروژن اکسید | نیتریک اکسید دینیتروژن تریاکسید نیتروژن دیاکسید دینیتروژن تترااکسید دینیتروژن پنتاکسید |
| ترکیبات مرتبط | آمونیوم نیترات آزید |
| به استثنای جایی که اشاره شدهاست در غیر این صورت، دادهها برای مواد به وضعیت استانداردشان داده شدهاند (در 25 °C (۷۷ °F)، ۱۰۰ kPa) | |
| | |
| Infobox references | |
|
| |
دینیتروژن مونوکسید یا نیتروز اکسید یا گاز خنده (N۲O) یکی از ترکیبات نیتروژن است که اولین بار در سال ۱۷۹۹ در دندانپزشکی استفاده شد. امروزه از آن در پزشکی برای القا و ادامهٔ بیهوشی استفاده میشود. این دارو همچنین با مقادیر مصرف کم بهعنوان ضد درد در اعمال جراحی زنان و زایمان و برای عمل جراحی که در آنها به بیهوشی کامل بیمار نیاز نیست، مصرف میشود. این گاز یک مادهٔ سایکو اکتیو از نوع منفک کننده است که در جوامع غربی به صورت گسترده به منظور ایجاد حس سرخوشی و توهم مورد مصرف قرار میگیرد بهطوری که تخمین زده میشود در سال ۲۰۱۴ توسط نیم میلیون جوان بریتانیایی مصرف شده باشد.[۱]
نیتروز اکسید (N۲O) گازی بیرنگ، بیبو و غیرقابل اشتعال است. N۲O سمّی نیست اما خندهآور است. این گاز در ردهٔ اصلی گازهای گلخانهای قرار داشته و آلوده کنندهٔ هوا میباشد. مطالعات اخیر نشان میدهد که این گاز میتواند باعث آسیب به سلولهای عصبی شود[۲] و پزشکان نسبت به مصرف آن در بین عموم هشدار دادهاند.[۳]
همچنین در موتورهای موشکی نیز کاربرد دارد اکسید نیتروژن ممکن است به عنوان یک اکسید کننده در موتور موشک استفاده شود. مزایایی نسبت به سایر اکسید کنندهها دارد زیرا سمی بسیار کمتری دارد و به دلیل پایداری در دمای اتاق ذخیرهسازی آسانتر و حمل در پرواز نسبتاً ایمن است. به عنوان یک مزیت ثانویه، ممکن است به راحتی تجزیه شود تا هوای تنفسی تشکیل شود. چگالی بالا و فشار ذخیرهسازی کم آن (زمانی که در دمای پایین نگهداری میشود) آن را قادر میسازد تا با سیستمهای ذخیرهسازی گاز فشار بالا رقابتی بالایی داشته باشد[۴]
در سال ۱۹۱۴، رابرت گدارد، پیشگام موشک آمریکایی، اکسید نیتروژن و بنزین را به عنوان پیشرانههای احتمالی برای موشکهای با سوخت مایع پیشنهاد کرد
اکسید نیتروژن اکسید کننده انتخابی در چندین طرح موشک هیبریدی (با استفاده از سوخت جامد با اکسید کننده مایع یا گاز) بودهاست. ترکیب اکسید نیتروژن با سوخت پلی بوتادین با پایانه هیدروکسیل توسط SpaceShipOne و دیگران استفاده شدهاست. همچنین بهطور قابل توجهی در موشکهای آماتور و پرقدرت با پلاستیکهای مختلف به عنوان سوخت استفاده میشود.
اکسید نیتروژن همچنین ممکن است در یک موشک تک پیشران استفاده شود. در حضور یک کاتالیزور گرم شده، N۲O در دمای تقریباً ۱۰۷۰ درجه فارنهایت (۵۷۷ درجه سانتیگراد) بهطور گرمازا به نیتروژن و اکسیژن تجزیه میشود
کاربرد در تقویت خودرو[ویرایش]
یکی از موارد کاربرد N۲O در تقویت خودرو است. دینیتروژن مونوکسید یک سوخت نیست که با سوختن آن در موتور اتومبیل بتوان انرژی تولید کرد. این گاز وقتی وارد سیلندر میشود، به دلیل گرمای زیاد داخل محفظه به اتم اکسیژن و نیتروژن تجزیه میگردد. در این تجزیه پیوند بین اتمها شکسته میشود. این عمل با گرفتن گرما از سیلندر همراه است در نتیجه دمای محفظهٔ احتراق کم میشود. خیلی سریع اتمهای فعال اکسیژن با هم ترکیب شده و مولکول O۲ را به وجود میآورند. حال اگر ما مقداری سوخت اضافی وارد سیلندر کنیم میتوانیم با گاز اکسیژن حاصله، سوخت اضافی را بسوزانیم و نیروی بیش تری تولید کنیم. توجه داشته باشید که سوزاندن سوخت اضافی زمانی ممکن میشود که دمای سیلندر پایین باشد و تجزیهٔ دینیتروژن مونوکسید این حالت را فراهم میآورد. در این فرایند گاز نیتروژن هیچ نقشی در انفجار نخواهد داشت!
N۲O در محفظههای تحت فشاری به نام Bottle Heaters یا Bottle Warmers در خودرو نگهداری میشود.
- فشار داخل این محفظه باید بین ۸۵۰ تا ۱۱۰۰ psi باشد تا بتواند گاز را در حالت مایع نگاه دارد. گاز از طریق لوله تحت فشار به مجرای تفس موتور (و یا خود سیلندر) تزریق میشود. به هنگام تزریق نیترو اکسید، این گاز از حالت مایع به گاز میرود چون نقطهٔ جوش آن در حدود منفی ۸۴ درجهٔ سانتی گراد است. در این تغییر فاز، دمای مخلوط هوا کاهش مییابد و در نتیجه فرایند انفجار بهتر صورت میگیرد.
تزریق به موتور[ویرایش]
نیترو اکسید به سه صورت به موتور تزریق میشود: ۱-تزریق خشک: در این حالت، گاز N۲O به تنهایی وارد مجرای تنفس میشود و سیستم سوخت رسانی به گونهای تنظیم میگردد که سوخت اضافی را وارد موتور کند.
۲-تزریق خیس: در این تزریق، گاز N۲O و سوخت اضافی ابتدا با هم مخلوط میشوند و از راه نازل وارد مجاری تنفس میگردند.
۳-تزریق مستقیم: در این حالت برای هر سیلندر یک تزریقکننده وجود دارد بهطوری که از هر یک از این نازلها، گاز N۲O به علاوهٔ سوخت اضافی وارد محفظهٔ احتراق میشود. این حالت بیش تر در خودروهای مخصوص مسابقه کاربرد دارد.
عمل تزریق با سوئیچهای کنترلی داخل خودرو انجام میشود که وصل شدن سوئیچ موجب فعال شدن سیم پیچ (سولنوئید)های مربوط به نیتروژن اکسید میگردد. یک کنترلر قابل برنامهریزی نیز حجم افزودن گاز نیترو اکسید را تعیین میکند. این کنترلکننده میتواند از نوع پیش رونده (Progressive) باشد که بهطور تصاعدی حجم گاز را افزایش میدهد یا از نوع دو مرحلهای باشد که طی دو مرحله حجم گاز را به حداکثر میرساند.
سیستم نیترو اکسید در تقویت خودرو اگر به درستی به کار گرفته شود، مشکلی برای موتور ایجاد نمیکند. این امر زمانی ممکن است که سیستم با ساختار موتور هماهنگ و از یک پک N۲O مناسب با تجهیزات حفاظتی استفاده شود.
منابع[ویرایش]
- ↑ "Warning over laughing gas misuse". The Guardian. 9 August 2014. Retrieved 9 August 2014.
- ↑ Winstock, Adam R.; Ferris, Jason A. (2020-02). "Nitrous oxide causes peripheral neuropathy in a dose dependent manner among recreational users". Journal of Psychopharmacology (Oxford, England). 34 (2): 229–236. doi:10.1177/0269881119882532. ISSN 1461-7285. PMID 31679459.
{{cite journal}}: Check date values in:|date=(help) - ↑ "Doctors warn of rise in nerve damage linked to nitrous oxide". the Guardian (به انگلیسی). 2022-08-30. Retrieved 2022-10-11.
- ↑ "Nitrous oxide". Wikipedia (به انگلیسی). 2022-07-09.
- فرهنگ داروهای ژنریک ایران، دکتر حشمتی، ۱۳۸۷
- ویکیپدیای انگلیسی
- Tuning Linx


 French
French Deutsch
Deutsch
