第IX因子
第IX因子(だい9いんし、英: factor IX、EC 3.4.21.22)は、凝固系を構成するセリンプロテアーゼの1つであり、クリスマス因子(Christmas factor)とも呼ばれる。ペプチダーゼファミリーS1に属し、このタンパク質の欠乏は血友病Bの原因となる。第IX因子は1952年に、Stephen Christmasという名前の少年がこの因子の欠損によって血友病を発症していることから発見された[5]。
第IX因子複合体製剤は、基本的な医療システムに必要な最重要医薬品のリストであるWHO必須医薬品モデル・リストに含まれている[6]。
生理学[編集]
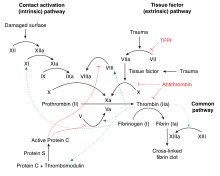
第IX因子は不活性な酵素前駆体として産生される。シグナルペプチドの除去とグリコシル化の後、第XIa因子(内因系)または第VIIa因子(外因系)によって切断されて2本鎖が産生される。両者はジスルフィド結合によって連結されている[7][8]。カルシウムイオン、膜のリン脂質、第VIII因子コファクターの存在下で第IXa因子へと活性化され、第X因子のアルギニン-イソロイシン間の結合を加水分解し第Xa因子を産生する。
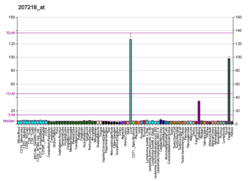
ヒトとマウスでは、第IX因子の発現は加齢に伴って上昇する。第IX因子のプロモーター領域に変異を有するマウスモデルでは年齢依存的な表現型が生じる[9]。
ドメイン構造[編集]
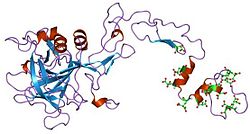
第VII因子、第IX因子、第X因子はすべて血液凝固に重要な役割を果たし、共通のドメイン構造を有する[10]。第IX因子は4つのドメインから構成され、Glaドメイン、タンデムに並んだ2コピーのEGFドメイン、切断を触媒するC末端のトリプシン様ペプチダーゼドメインからなる。

N末端のEGFドメインは、少なくとも部分的には組織因子との結合を担うことが示されている[10]。Wilkinsonらは、2番目のEGFドメインの88番から109番残基が血小板への結合と第X因子活性化複合体の組み立てを媒介すると結論付けている[11]。
4つのドメイン全ての構造が解かれている。2つのEGFドメインとトリプシン様ドメインの構造はブタ由来のタンパク質で決定されている[12]。Ca2+依存的なリン脂質結合を担うGlaドメインの構造もNMRによって決定されている[13]。
いくつかの「超活性型」変異体の構造も解かれており[14]、血液凝固カスケードの他のタンパク質による第IX因子活性化の性質が明らかにされている。
遺伝子[編集]

第IX因子の遺伝子はX染色体(Xq27.1-q27.2)に位置しており、そのため、この遺伝子の変異は女性よりもはるかに高頻度で男性に影響を与える。倉地幸徳とEarl Davieによって1982年に初めてクローニングされた[15]。
ヒトの第IX因子の遺伝子を持つトランスジェニッククローンのヒツジポリーが、1997年にロスリン研究所のイアン・ウィルムットによって作製された[16]。
疾患における役割[編集]
第IX因子の欠乏はクリスマス病(血友病B)を引き起こす[5]。これまでに第IX因子の100以上の変異が記載されており、一部は無症状であるが、多くは重症の出血性疾患を引き起こす。元々のクリスマス病変異はクリスマス少年のDNAのシーケンシングによって同定され、システインがセリンへ置換されていることが明らかにされた[17]。クリスマス病の治療には組換え第IX因子が利用されている。組換え第IX因子製剤としては次のようなものがある。
- ノナコグアルファ(nonacog alfa、商標名ベネフィックス(BeneFix))[18]
- アルブトレペノナコグアルファ(albutrepenonacog alfa、商標名イデルビオン(Idelvion))[19]
- エフトレノナコグアルファ(eftrenonacog alfa、商標名オルプロリクス(Alprolix))[20]
一部の稀な変異は凝固活性を上昇させ、そのため深部静脈血栓症などの凝固障害が引き起こされる。この機能獲得型変異ではタンパク質が機能過剰となり、家族性・早発性の血栓症と関連している[21]。
第IX因子欠乏症は、さまざまな動物や動物細胞でのクローニングによって産生された、精製第IX因子の注入によって治療が行われる。トラネキサム酸は、周術期の出血リスクを低下させるため、遺伝性第IX因子欠乏症の患者が手術を行う際には有用である可能性がある[22]。
第IX因子の全ての変異のリストは、ユニヴァーシティ・カレッジ・ロンドンで管理されているFactor IX mutation databaseに集められ管理される[23]。
出典[編集]
- ^ a b c GRCh38: Ensembl release 89: ENSG00000101981 - Ensembl, May 2017
- ^ a b c GRCm38: Ensembl release 89: ENSMUSG00000031138 - Ensembl, May 2017
- ^ Human PubMed Reference:
- ^ Mouse PubMed Reference:
- ^ a b “Christmas disease: a condition previously mistaken for haemophilia”. British Medical Journal 2 (4799): 1378–82. (Dec 1952). doi:10.1136/bmj.2.4799.1378. PMC 2022306. PMID 12997790.
- ^ “19th WHO Model List of Essential Medicines (April 2015)”. WHO (2015年4月). 2015年5月10日閲覧。
- ^ a b “Activation of human factor IX (Christmas factor)”. The Journal of Clinical Investigation 61 (6): 1528–38. (Jun 1978). doi:10.1172/JCI109073. PMC 372679. PMID 659613.
- ^ “Factor IX of the blood coagulation system: a review”. Biochemistry. Biokhimiia 62 (7): 685–93. (Jul 1997). PMID 9331959.
- ^ “Age-specific regulation of clotting factor IX gene expression in normal and transgenic mice”. Blood 86 (6): 2198–205. (Sep 1995). PMID 7662969.
- ^ a b “The N-terminal epidermal growth factor-like domain in factor IX and factor X represents an important recognition motif for binding to tissue factor”. The Journal of Biological Chemistry 277 (5): 3622–31. (Feb 2002). doi:10.1074/jbc.M111202200. PMID 11723140.
- ^ “The factor IXa second epidermal growth factor (EGF2) domain mediates platelet binding and assembly of the factor X activating complex”. The Journal of Biological Chemistry 277 (8): 5734–41. (Feb 2002). doi:10.1074/jbc.M107753200. PMID 11714704.
- ^ “X-ray structure of clotting factor IXa: active site and module structure related to Xase activity and hemophilia B”. Proceedings of the National Academy of Sciences of the United States of America 92 (21): 9796–800. (Oct 1995). doi:10.1073/pnas.92.21.9796. PMC 40889. PMID 7568220.
- ^ “Structure of the calcium ion-bound gamma-carboxyglutamic acid-rich domain of factor IX”. Biochemistry 34 (38): 12126–37. (Sep 1995). doi:10.1021/bi00038a005. PMID 7547952.
- ^ “Structural basis of the cofactor- and substrate-assisted activation of human coagulation factor IXa”. Structure 17 (12): 1669–78. (Dec 2009). doi:10.1016/j.str.2009.10.011. PMID 20004170.
- ^ “Isolation and characterization of a cDNA coding for human factor IX”. Proceedings of the National Academy of Sciences of the United States of America 79 (21): 6461–4. (Nov 1982). doi:10.1073/pnas.79.21.6461. PMC 347146. PMID 6959130.
- ^ Nicholl D. (2002). An Introduction to Genetic Engineering Second Edition. Cambridge University Press. p. 257
- ^ “Characterization of the original Christmas disease mutation (cysteine 206----serine): from clinical recognition to molecular pathogenesis”. Thrombosis and Haemostasis 67 (1): 63–5. (Jan 1992). doi:10.1055/s-0038-1648381. PMID 1615485.
- ^ “Home: BeneFIX Coagulation Factor IX (Recombinant) Official Site”. 2019年11月17日閲覧。
- ^ “Factor IX Therapy for Hemophilia B | IDELVION coagulation factor IX (recombinant), albumin fusion protein”. www.idelvion.com. 2019年11月17日閲覧。
- ^ “Home: Alprolix [Coagulation Factor IX (Recombinant), Fc Fusion Protein Official Site]”. 2019年11月17日閲覧。
- ^ “X-linked thrombophilia with a mutant factor IX (factor IX Padua)”. The New England Journal of Medicine 361 (17): 1671–5. (Oct 2009). doi:10.1056/NEJMoa0904377. PMID 19846852.
- ^ “Do patients with haemophilia undergoing cardiac surgery have good surgical outcomes?”. Interactive Cardiovascular and Thoracic Surgery 13 (3): 320–31. (Sep 2011). doi:10.1510/icvts.2011.272401. PMID 21712351.
- ^ “Home: Factor IX Mutation Database”. 2019年11月17日閲覧。
関連文献[編集]
- “Basic mechanisms in blood coagulation”. Annual Review of Biochemistry 44: 799–829. (1975). doi:10.1146/annurev.bi.44.070175.004055. PMID 237463.
- “Assessing the underlying pattern of human germline mutations: lessons from the factor IX gene”. FASEB Journal 6 (10): 2767–74. (Jul 1992). doi:10.1096/fasebj.6.10.1634040. PMID 1634040.
- “The life cycle of coagulation factor VIII in view of its structure and function”. Blood 92 (11): 3983–96. (Dec 1998). PMID 9834200.
- “Factor IX and thrombosis”. British Journal of Haematology 115 (3): 507–13. (Dec 2001). doi:10.1046/j.1365-2141.2001.03186.x. PMID 11736930.
- “Factor XI deficiency--from molecular genetics to clinical management”. Blood Coagulation & Fibrinolysis 14 Suppl 1: S59-64. (Jun 2003). doi:10.1097/00001721-200306001-00014. PMID 14567539.
- “Signaling and regulation of the platelet glycoprotein Ib-IX-V complex”. Current Opinion in Hematology 14 (3): 262–9. (May 2007). doi:10.1097/MOH.0b013e3280dce51a. PMID 17414217.
外部リンク[編集]
- GeneReviews/NCBI/NIH/UW entry on Hemophilia B
- MEROPS ペプチダーゼとその阻害剤についてのオンラインデータベース: S01.214


 French
French Deutsch
Deutsch