流動モザイクモデル
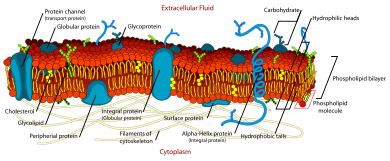
流動モザイクモデル(りゅうどうモザイクモデル、英: fluid mosaic model)は、機能的な細胞膜の構造に関するさまざまな知見を説明するモデルである。このモデルによると、細胞膜はタンパク質分子が埋め込まれた脂質二重層である。脂質二重層は膜へ流動性と弾性を与える。このモデルは1972年にシーモア・ジョナサン・シンガーとガース・L・ニコルソンによって考案されたもので、細胞膜はリン脂質とタンパク質分子が容易に拡散する二次元液体であると説明される[1]。膜の構成要素の横方向への拡散を制限する膜ドメインの重要性が新たに発見され、これらの知見を説明するためにモデルは更新されている。このような膜ドメインは、脂質ラフト、またはタンパク質や糖タンパク質の複合体の形成を促進する特別な脂質やタンパク質の組成を持つ領域として定義される。膜ドメインは、細胞骨格繊維や細胞外マトリックスとの膜タンパク質を介した結合によっても定義される[2]。現行のモデルは、細胞シグナル伝達、アポトーシス、細胞分裂、膜の出芽、細胞融合など、多くの細胞過程に関連する重要な特徴を説明することができ、細胞膜のモデルとして最も受け入れられている。
化学的構成[編集]
細胞膜は化学的には、リン脂質、タンパク質、炭水化物、コレステロールという4つの要素から構成される。
実験的証拠[編集]
機能的な生体膜の持つ流動的性質は、スピンラベリング、X線回折、カロリメトリー実験を通じて示されてきた。これらの研究によって、膜タンパク質の拡散速度は自らが埋め込まれた脂質二重層の粘度の影響を受けることが示され、細胞膜内の分子は静的ではなく動的であることが実証された[1]。
以前の生体膜のモデルとしては、J. David Robertsonによる単位膜モデルやダブソン–ダニエリモデルがあった[2]。これらのモデルでは、タンパク質はリン脂質の二重層に取り込まれているのではなく、脂質層に隣接したシートとして存在しているとされた。他のモデルでは、タンパク質と脂質の層が規則正しく繰り返されているとされた。これらのモデルは顕微鏡的・熱力学的なデータによる支持があまり得られず、膜の動的な性質の証拠を取り入れることもできなかった[2]。

生体膜の流動的性質を支持する証拠となる重要な実験はFryeとEdidinによって行われた。彼らは、センダイウイルスを用いてヒトとマウスの細胞を融合させ、ヘテロカリオンを形成させた。マウスとヒトのタンパク質は、細胞融合の直後はヘテロカリオンの各半球に分かれて位置していることが抗体染色によって示された。しかし、タンパク質は徐々に拡散し、時間と共に両半球の境界は失われた。温度を下げることで膜のリン脂質の流体相からゲル相への転移が引き起こされ、拡散の速度は低下した[3]。シンガーとニコルソンは、流動モザイクモデルを用いてこれらの実験の結果を合理的に説明した[1]。
流動モザイクモデルは、細胞膜の構造と性質の温度による変化や、膜と膜タンパク質の結合の説明が可能であった。シンガーとニコルソンは自らのモデルを支持する多くの証拠を複数の分野から得ていたが、近年の蛍光顕微鏡や構造生物学の進展によって細胞膜の流動モザイク性は確証された。
その後の発展[編集]
膜の非対称性[編集]
生体膜の2つの層は非対称的で、さらに特定のタンパク質や脂質組成によって構成されるサブドメインへと分割される。これによって、膜と関連した生物学的過程を空間的に分離することが可能となっている。コレステロールとコレステロール結合タンパク質は脂質ラフトに集中しており、これらのラフトに限定された細胞シグナリングが行われる[4]。他の非対称性はMouritsenとBloomによって1984年に示された。彼らは脂質-タンパク質間相互作用によって脂質膜の厚さやタンパク質の疎水性領域の長さが変化するというマットレスモデル(Mattress model)を提唱した[5]。
二重層ではない膜[編集]
流動モザイクモデルの発表後、重要な生物学的機能を持つ、二重膜ではない脂質構成の存在が確認された。これらの膜構造は細胞分裂や密着結合の形成時にみられ、細胞が非二重層構造を拡大する必要がある時に有用である可能性がある[6]。
膜の湾曲[編集]
膜の二重層は常に平坦であるわけではない。局所的な膜の湾曲は、上述した非対称的な脂質組成や非二重層構造によって引き起こされる。より劇的で機能的な湾曲がBARドメインによって行われる。BARドメインは膜表面のホスファチジルイノシトールに結合し、小胞や細胞小器官の形成、細胞分裂を助ける[7]。常に流動的に湾曲は形成され続けており、生体膜の動的な性質に寄与している[8]。
膜内の脂質の移動[編集]
1970年代に、個々の脂質分子は脂質膜の各層内を横方向に自由に拡散することが明らかにされた[9]。平均的な脂質分子は1秒で約 2 µmと高速で拡散し、これは大きな細菌の細胞の長さに相当する[9]。また個々の脂質分子が自身の軸に沿って高速で回転していることも観察された[9]。さらにリン脂質分子は、稀にではあるが、一方の層から他方の層へ移動する(フリップフロップ(flip-flop)として知られる)。しかし、フリップフロップはフリッパーゼと呼ばれる酵素によって増強されたものである可能性がある。上述したこれらの過程は、脂質分子と脂質膜内で相互作用するタンパク質の無秩序性に影響し、膜の流動性やシグナル伝達、輸送、機能に影響をもたらしている。
二重層の流動性の制限[編集]
脂質やタンパク質要素の横方向の移動性は、脂質二重層内でのサブドメインの形成によって制限される。これらのサブドメインは、膜要素の細胞外マトリックスへの結合などのいくつかの過程や、またはタンパク質複合体や脂質ラフトの形成を促進するような特定の生化学的組成を持つナノメートルスケールの膜領域などによって生じる[2]。さらに、タンパク質と細胞骨格の接着によって“cytoskeletal fences”が形成される。この柵の内部では脂質や膜タンパク質は自由に拡散するが、そこから外部へ離れることはめったに起こらない[2]。膜要素の横方向の拡散速度の制限によって細胞膜の特定の領域に特定の機能を付与することが可能となるため、これらは極めて重要である。
脂質ラフト[編集]
脂質ラフトは、特定の脂質とタンパク質組成を有するナノメートルスケールの領域であり、横方向に拡散し脂質二重層上を移動する。スフィンゴリン脂質とコレステロールは、脂質ラフトの重要な構成要素である[10]。
タンパク質複合体[編集]
細胞膜のタンパク質や糖タンパク質は、シンガーとニコルソンが1972年に最初に提唱したように脂質膜に単独の要素として存在しているのではない。むしろ、膜内を拡散する複合体として存在している[2]。このような高分子複合体への集合は、イオンや代謝産物の輸送、シグナル伝達、細胞接着、細胞遊走といった重要な細胞機能をもたらしている[2]。
cytoskeletal fencesと細胞外マトリックスへの結合[編集]
脂質二重膜に埋め込まれたタンパク質の一部は、細胞外マトリックス、細胞内の細胞骨格繊維、セプチンのリング状構造と相互作用している。これらの相互作用は、細胞の形状や構造、区画化に強い影響を与えている。さらにこれらは、タンパク質と一部の脂質の二重膜内の横方向の拡散に対する物理的な障壁となっている[2]。
膜へ埋め込まれたタンパク質が細胞外マトリックスへ結合しているとき、それらは自由に拡散することはできない。また、長い細胞内ドメインを持つタンパク質は、細胞骨格繊維によって形成された柵(cytoskeletal fences)と衝突する[11]。どちらの過程もタンパク質と結合脂質の拡散を制限し、それらと相互作用している細胞膜の要素も同様に拡散が制限される。

セプチンはGTP結合タンパク質のファミリーで、真核生物で高度に保存されている。原核生物もパラセプチン(paraseptin)と呼ばれる類似したタンパク質を有している。これらは細胞膜と強く結合したリング状構造を形成し、細胞を区画化する。セプチンは、繊毛、鞭毛、樹状突起スパイン、酵母の出芽構造などの形成に関与している[12]。
歴史年表[編集]
- 1895年 – アーネスト・オーバートンは、細胞膜が脂質で作られているという仮説を立てた[13]。
- 1925年 – Evert GorterとFrançois Grendelは赤血球の膜が2分子の厚さの脂質の層で形成されていることを発見し、細胞膜の脂質二重層について記述した[14]。
- 1935年 – ヒュー・ダブソンとジェームス・ダニエリは、脂質膜はタンパク質で構成される層であり、特定の物質を透過させる孔を持つ構造であると提唱した。その後彼らは、脂質の層の両側がタンパク質の層で囲まれた細胞膜のモデルを提唱した[15]。
- 1957年 – J. David Robertsonは、電子顕微鏡の研究に基づいて「単位膜仮説」(Unit Membrane Hypothesis)を提唱した。この説では、細胞内の全ての膜、つまり細胞膜も細胞小器官の膜も同じ構造を持っており、リン脂質の二重層の両側にタンパク質の単層が存在するとされた[16]。
- 1972年 – シンガーとニコルソンは、細胞膜の構造や熱力学に関する最新のデータを説明するモデルとして、流動モザイクモデルを提唱した[1]。
出典[編集]
- ^ a b c d “The fluid mosaic model of the structure of cell membranes”. Science 175 (4023): 720–31. (Feb 1972). doi:10.1126/science.175.4023.720. PMID 4333397.
- ^ a b c d e f g h Nicolson GL (2014). “The Fluid—Mosaic Model of Membrane Structure: Still relevant to understanding the structure, function and dynamics of biological membranes after more than 40 years”. Biochimica et Biophysica Acta 1838 (6): 1451–146. doi:10.1016/j.bbamem.2013.10.019. PMID 24189436.
- ^ “The rapid intermixing of cell surface antigens after formation of mouse-human heterokaryons”. J Cell Sci 7 (2): 319–35. (1970). PMID 4098863.
- ^ Silvius JR (2005). “Partitioning of membrane molecules between raft and non-raft domains: Insights from model-membrane studies”. Biochimica et Biophysica Acta 1746 (3): 193–202. doi:10.1016/j.bbamcr.2005.09.003. PMID 16271405.
- ^ “Mattress model of lipid-protein interactions in membranes”. Biophys J 46 (2): 141–153. (1984). doi:10.1016/S0006-3495(84)84007-2. PMC 1435039. PMID 6478029.
- ^ van den Brink-van der Laan E (2004). “Nonbilayer lipids affect peripheral and integral membrane proteins via changes in the lateral pressure profile”. Biochim Biophys Acta 1666 (1–2): 275–88. doi:10.1016/j.bbamem.2004.06.010. PMID 15519321.
- ^ Frost A (2009). “The BAR domain superfamily: membrane-molding macromolecules”. Cell 137 (2): 191–6. doi:10.1016/j.cell.2009.04.010. PMC 4832598. PMID 19379681.
- ^ Rodríguez-García R (2009). “Bimodal spectrum for the curvature fluctuations of bilayer vesicles: pure bending plus hybrid curvature-dilation modes”. Phys Rev Lett 102 (12): 128101. doi:10.1103/PhysRevLett.102.128101. PMID 19392326.
- ^ a b c Molecular Biology of the Cell (5th ed.). New York: Garland Science. (2008). pp. 621–622. ISBN 978-0-8153-4105-5
- ^ “Lipid rafts as a membrane-organizing principle”. Science 327 (5961): 46–50. (2010). doi:10.1126/science.1174621. PMID 20044567.
- ^ G. Vereb (2003). “Dynamic, yet structured: The cell membrane three decades after the Singer–Nicolson model”. PNAS 100 (14): 8053–8058. doi:10.1073/pnas.1332550100. PMC 166180. PMID 12832616.
- ^ Juha Saarikangas; Yves Barral (2011). “The emerging functions of septins in metazoans”. EMBO Reports 12 (11): 1118–1126. doi:10.1038/embor.2011.193. PMC 3207108. PMID 21997296.
- ^ Overton, E (1895). “Uberdie osmotischen Eigenshafter der Lebenden Pflanzen und tierzelle”. VJSCHR Naturf Ges Zurich 40: 159–201.
- ^ E. Gorter; F. Grendel (1925). “On Biomolecular Layers of Lipoids on the Chromocytes of the Blood”. Journal of Experimental Medicine 41 (4): 439–443. doi:10.1084/jem.41.4.439. PMC 2130960. PMID 19868999.
- ^ James Danielli; Hugh Davson (1935). “A contribution to the theory of permeability of thin films”. Journal of Cellular and Comparative Physiology 5 (4): 495–508. doi:10.1002/jcp.1030050409.
- ^ John E. Heuser (1995). “In Memory of J. David Robertson”. Newsletter of the American Society of Cell Biology.


 French
French Deutsch
Deutsch