Elektrokardiografia – Wikipedia, wolna encyklopedia
| Ten artykuł należy dopracować |

Elektrokardiografia (EKG) – zabieg diagnostyczny wykorzystywany w medycynie przede wszystkim w celu rozpoznawania chorób serca.
Pomijając EKG wykonywane w czasie operacji na sercu, jest to metoda pośrednia polegająca na rejestracji elektrycznej czynności mięśnia sercowego z powierzchni klatki piersiowej w postaci różnicy potencjałów (napięć) pomiędzy dwiema elektrodami, co graficznie odczytujemy w formie krzywej elektrokardiograficznej, na specjalnym papierze milimetrowym bądź na ekranie monitora.
EKG nie jest niezawodnym kryterium rozpoznania choroby: istnieje możliwość prawidłowego elektrokardiogramu przy schorzeniach kardiologicznych oraz nieprawidłowy zapis czynności elektrycznej przy prawidłowym stanie klinicznym.

Historia elektrokardiografii[edytuj | edytuj kod]


Historia EKG – szczególnie w swoich początkach – wiąże się z odkryciami z dziedziny fizyki, gdyż elektrokardiograf w istocie jest bardzo czułym galwanometrem. Późniejszy rozwój EKG związany jest z obserwacją zmian pojawiających się w zapisie i ich powiązaniem z konkretnymi jednostkami chorobowymi.
W 1819 r. duński fizyk Hans Christian Ørsted podczas demonstracji studentom ogrzewania platynowego drutu prądem z ogniwa Volty, zauważył, że igła magnetyczna leżącego obok kompasu porusza się za każdym razem gdy prąd elektryczny jest włączony. W ten sposób odkrył elektromagnetyzm.
W 1820 r. Johann Schweigger zwiększył poruszanie się igieł magnetycznych w polu elektromagnetycznym. Odkrył, że przez 100-krotne owinięcie drutu z prądem na szpulce, oddziaływanie na igłę ulega zwiększeniu. Schweigger wynalazł pierwszy galwanometr i ogłosił swój wynalazek na Uniwersytecie Halle 16 września 1820.
W 1842 r. Carlo Matteucci, profesor fizyki na Uniwersytecie w Pizie, pokazał, że prąd elektryczny towarzyszy każdemu uderzeniu serca żaby.
W 1872 r. francuski fizyk Gabriel Lippmann wynalazł elektrometr kapilarny. Jest to cienka szklana rurka ze słupem rtęci pod kwasem siarkowym. Menisk rtęci przesuwa się wraz ze zmianami potencjałów elektrycznych i jest obserwowany pod mikroskopem.
W 1876 r. Marey użył elektrometru do zapisu aktywności elektrycznej eksponowanego serca żaby.
W 1878 r. brytyjscy fizjolodzy John Burden Sanderson i Friderick Page zapisali prąd elektryczny serca żaby przy użyciu kapilarnego elektrometru i pokazali, że zapis ten składa się z dwóch faz (później nazwanych QRS i T).
W 1880 r. francuski fizyk Jacques-Arsène d’Arsonval we współpracy z Marcelem Deprezem ulepszył galwanometr. Zamiast igły magnetycznej poruszającej się gdy prąd elektryczny przepływał przez otaczającą drucianą zwojnicę, galwanometr Deprez-d’Arsonval miał zamocowany na stałe magnes i ruchome uzwojenie. Jeśli wskaźnik był przymocowany do zwojnicy, to mógł się on poruszać na odpowiedniej skali. Galwanometr d'Arsonvala stał się podstawą dla najnowocześniejszych galwanometrów.
W 1887 r. brytyjski fizjolog Augustus D. Waller ze Szkoły Medycznej St Mary w Londynie opublikował pierwszy ludzki elektrokardiogram. Został on wykonany na techniku laboratoryjnym przy użyciu elektrometru kapilarnego.
W 1889 r. holenderski fizjolog Willem Einthoven zobaczył demonstrowaną przez Wallera technikę na I Międzynarodowym Kongresie Fizjologów w Bale. Z czasem to właśnie Einthoven stanie się kluczową osobą w rozwoju elektrokardiografii.
W 1890 r. G.J. Burch z Oksfordu wymyślił arytmetyczną poprawkę dla obserwowanych fluktuacji elektrometru. Pozwoliło to zobaczyć prawdziwy kształt fali, ale wymagało męczących obliczeń.
W 1891 r. brytyjscy fizjolodzy William Bavliss i Edward Starling z Kolegium Uniwersyteckiego w Londynie ulepszyli elektrometr kapilarny. Połączyli koniec do prawej ręki i do skóry nad uderzeniem koniuszkowym i pokazali „trójfazową zmianę towarzyszącą (czy raczej poprzedzającą) każdemu uderzeniu serca”.
W 1893 r. Willem Einthoven wprowadził termin elektrokardiogram na spotkaniu Holenderskiego Stowarzyszenia Medycznego (później zgłoszono pretensje, że Waller pierwszy użył tego określenia).
W 1895 r. Einthoven, używając ulepszonego elektrometru i formułę poprawki, odkrył rozróżnienie 5 wychyleń, które nazwał P, Q, R, S i T.
W 1899 r. Karel Frederik Wenckebach opublikował artykuł O analizie nieregularnych pulsów opisujący osłabienie przewodnictwa przedsionkowo-komorowego prowadzącą do progresywnego wydłużenia i blokady przewodzenia przedsionkowo-komorowego u żaby. Nazwano to później blokiem Wenckebacha (Mobitz typu I) lub fenomenem Wenckebacha (periodyku Wenckebacha).
Ponieważ Einthoven zdawał sobie sprawę, że rejestracja zapisów elektrokardiograficznych przy użyciu elektrometru kapilarnego i formuły poprawki jest na tyle czasochłonna i uciążliwa, że nie nadaje się do zastosowania na szerszą skalę, zwrócił swoją uwagę na możliwość zastosowania w tym celu galwanometrów. Miały one jednak istotną niedogodność – były zbyt mało czułe. W 1901 r. Einthoven skonstruował nowy galwanometr do wykonywania elektrokardiogramu, używając drobnej kwarcowej struny pokrytej srebrem, inspirując się pomysłem Depreza i d'Arnsovala (którzy użyli drucianego uzwojenia). Jego galwanometr strunowy ważył 600 funtów.
W 1902 r. Einthoven opublikował pierwszy elektrokardiogram zapisany na galwanometrze strunowym. Już w 1903 r. Einthoven dyskutował o możliwości komercyjnej produkcji galwanometru strunowego z Maxem Edelmannem z Monachium i Horace Darwinem z londyńskiego Cambridge Scientific Instruments Company.
W 1905 r. Einthoven rozpoczął przesyłanie elektrokardiogramu ze szpitala do swojego laboratorium oddalonego o 1,5 km przez kabel telefoniczny. W 1906 Einthoven opublikował pierwszą uporządkowaną prezentację prawidłowych i nieprawidłowych zapisów elektrokardiograficznych na galwanometrze strunowym. Zostały opisane: przerost lewej i prawej komory, przerost lewego i prawego przedsionka, fala U (po raz pierwszy), załamki QRS, przedwczesne skurcze komorowe, bigeminia komorowa, trzepotanie przedsionków i całkowity blok sercowy.
W 1906 r. Cremer zapisał pierwszy elektrokardiogram przełykowy, który wykonał za pomocą sondy przełykowej. Elektrokardiografia przełykowa rozwinęła się dopiero w latach 70. XX wieku jako pomocna w różnicowaniu niemiarowości przedsionkowych. Cremer zapisał również pierwszy elektrokardiogram płodu z powierzchni brzucha ciężarnej kobiety.
W 1908 r. Edward Schafer z uniwersytetu w Edynburgu po raz pierwszy kupił galwanometr strunowy do celów klinicznych. W 1909 Nicolai i Simmons donieśli o zmianach elektrokardiogramu podczas dusznicy bolesnej.
W 1911 r. Thomas Lewis opublikował klasyczny skrypt Mechanizm bicia serca i zadedykował go Willemowi Einthovenowi.
W 1912 r. Einthoven opisał trójkąt równoboczny utworzony przez standardowe odprowadzenia I, II i III, później nazwany trójkątem Einthovena.
W 1920 r. Harold Pardee z Nowego Jorku opublikował pierwszy elektrokardiogram świeżego zawału serca u człowieka i opisał załamek T.
W 1924 r. Einthoven otrzymał Nagrodę Nobla w dziedzinie fizjologii lub medycyny za odkrycie zasady elektrokardiogramu.
Również w 1924 r. Woldemar Mobitz opublikował swoją klasyfikację bloków serca (Mobitz typu I i II) opartą na zapisie elektrokardiogramu i kształcie fali tętna żyły szyjnej badanej u pacjentów z blokiem sercowym drugiego stopnia.
W 1928 r. Ernstine i Levine donieśli o zastosowaniu lamp elektronowych do wzmocnienia elektrokardiogramu zamiast mechanicznego wzmacniania w galwanometrze strunowym.
W 1928 r. zakłady Franka Sanborna zmieniły swój model stołowy maszyny elektrokardiograficznej na pierwszą wersję nadającą się do przenoszenia ważącą 50 funtów i zasilaną 6 V akumulatorem samochodowym.
W 1930 r. Wolff, Parkinson i White donieśli o zespole elektrokardiograficznym krótkiego odcinka PR, szerokiego QRS i napadowej tachykardii.
W 1930 r. Sanders opisał jako pierwszy zawał prawej komory.
W 1931 r. Charles Wolferth i Francis Wood opisali zastosowanie ćwiczeń fizycznych do wywołania napadu dusznicy bolesnej. Badali oni zmiany EKG u zdrowych osób i tych z dusznicą, ale odrzucili tę technikę jako zbyt niebezpieczną. Natomiast w 1932 Goldhammer i Scherf zaproponowali użycie elektrokardiogramu po umiarkowanych ćwiczeniach jako pomoc w diagnostyce niewydolności wieńcowej.
W 1932 r. Charles Wolferth i Francis Wood opisali kliniczne zastosowanie odprowadzeń sercowych.
W 1934 r. przez połączenie drutów do prawego i lewego ramienia oraz lewej stopy z opornikiem 5000 omów Frank Wilson zdefiniował elektrodę obojętną później nazwaną Wilson Central Terminal. Kombinacja odprowadzeń działała jak uziemienie i była związana z ujemnym końcem EKG. Elektroda związana z dodatnim końcem później stała się „jednobiegunową” i mogła być umiejscowiona gdziekolwiek na ciele. Wilson określił jednobiegunowe odprowadzenia VR, VL i VF gdzie „V” było związane z napięciem (napięcie widoczne w miejscu jednobiegunowej elektrody).
W 1938 r. American Heart Association i Cardiac Society z Wielkiej Brytanii zdefiniowały standardowe umiejscowienie i przewody elektryczne odprowadzeń przedsercowych V1-V6. „V” oznacza napięcie.
W 1942 r. Emanuel Goldberger zwiększył napięcie jednobiegunowych odprowadzeń Wilsona o 50% i utworzył zwiększone odprowadzenia kończynowe aVR, aVL i aVF. Po dodaniu trzech odprowadzeń kończynowych i 6 odprowadzeń piersiowych otrzymamy 12-odprowadzeniowy elektrokardiogram, który jest obecnie używany.
Również w 1942 r. Artur Master standaryzował dwukrokowy test wysiłkowy funkcji serca (znany obecnie jako Master two-step).
W 1949 r. Sokolow i Lyon zaproponowali diagnostyczne kryteria przerostu lewej komory tj. ma ona miejsce, gdy suma wielkości załamka S w V1 i załamka R w V6 przekracza 35 mm.
W 1959 r. Myron Prinzmetal opisał odmienną postać dusznicy, w której odcinek ST jest raczej podwyższony niż obniżony.
W 1960 r. Smirk i Palmer uwydatnili ryzyko nagłej śmierci z powodu migotania komór szczególnie gdy komorowe skurcze przedwczesne zachodzą w tym samym czasie co załamek T. Fenomen „R na T”.
W 1963 r. Robert Bruce i wsp. opisali wieloetapowy test wysiłkowy na bieżni, znany później jako protokół Bruce'a.
W 1963 r. Baule i McFee byli pierwszymi, którzy odkryli magnetokardiogram, będący polem elektromagnetycznym powstającym z powodu aktywności elektrycznej serca. Jest to metoda mogąca wykonywać EKG bez użycia elektrod skórnych. Chociaż potencjalnie była to technika użyteczna nigdy nie uzyskała klinicznej akceptacji, m.in. z powodu wyższych kosztów.
W 1968 r. Henry Marriott wprowadził zmodyfikowane odprowadzenie piersiowe 1 (MCL 1) do monitorowania pacjentów intensywnego nadzoru kardiologicznego.
W 1976 r. Erhard i wsp. opisali użycie prawostronnego odprowadzenia przedsercowego do diagnostyki zawału prawej komory, który wcześniej był dla elektrokardiografii utajony.
W 1993 r. Robert Zalenski, profesor medycyny ratunkowej z Uniwersytetu Stanowego Wayne w Detroit i wsp. opublikowali artykuł na temat klinicznego użycia 15-odprowadzeniowego EKG z rutynowym stosowaniem V4R, V8 i V9 w diagnostyce ostrych zespołów wieńcowych. Podobnie jak dodane 6 standaryzowanych jednobiegunowych odprowadzeń przedsercowych w 1938 r. te dodatkowe odprowadzenia zwiększą czułość elektrokardiogramu w wykrywaniu zawału serca.
Dlaczego PQRST[edytuj | edytuj kod]
5 wychyleń rejestrowanych na zapisie EKG przed wprowadzeniem w 1890 r. formuły poprawki oznaczano ABCDE, natomiast 5 pochodnych wychyleń oznaczono PQRST. Wybór P jest matematyczną konwencją na używanie liter z drugiej połowy alfabetu. N ma inne znaczenie w matematyce, a O jest używane jako początek kartezjańskiego układu współrzędnych. Ponadto Einthoven użył O...X do zaznaczenia linii czasowych na swoim diagramie. P jest po prostu następną literą.
Historia odprowadzeń EKG[edytuj | edytuj kod]
Standardowe odprowadzenia I, II, III zostały zaproponowane przez Einthovena, który w 1912 r. przy ich pomocy wyznaczył obecnie tzw. „trójkąt Einthovena”. W 1934 r. przez połączenie drutów do prawego i lewego ramienia oraz lewej stopy z opornikiem 5000 omów Frank Wilson zdefiniował „elektrodę obojętną”. Kombinacja odprowadzeń działała jak uziemienie i była związana z ujemnym końcem EKG. Elektroda związana z dodatnim końcem później stała się „jednobiegunową” i mogła być umiejscowiona gdziekolwiek na ciele. Wilson określił jednobiegunowe odprowadzenia VR, VL i VF gdzie „V” było związane z napięciem (napięcie widoczne w miejscu jednobiegunowej elektrody). W 1938 r. American Heart Association i Cardiac Society z Wielkiej Brytanii zdefiniowały standardowe umiejscowienie i przewody elektryczne odprowadzeń przedsercowych V1-V6. „V” oznacza napięcie. W 1942 r. Emanuel Goldberger zwiększył napięcie jednobiegunowych odprowadzeń Wilsona o 50% i utworzył zwiększone odprowadzenia kończynowe aVR, aVL i aVF. Po dodaniu trzech odprowadzeń kończynowych i 6 odprowadzeń piersiowych otrzymamy 12-odprowadzeniowy elektrokardiogram, który jest obecnie używany. W 1968 r. Henry Marriott wprowadził zmodyfikowane odprowadzenie piersiowe 1 (MCL 1) do monitorowania pacjentów intensywnego nadzoru kardiologicznego. W 1993 Robert Zalenski zaproponował kliniczne zastosowanie 15-odprowadzeniowego EKG z rutynowymi odprowadzeniami V4R, V8 i V9.
Podstawa elektrofizjologiczna EKG[edytuj | edytuj kod]
Potencjał spoczynkowy[edytuj | edytuj kod]
Elektrokardiogram jest graficznym zapisem zmian potencjałów w trakcie depolaryzacji i repolaryzacji komórek mięśnia sercowego. Na poziomie pojedynczego kardiomiocytu zmiany elektryczne prezentują się następująco, a ich znajomość jest niezbędna, by zrozumieć charakterystyczne zmiany potencjału krzywej EKG (załamki, odstępy, odcinki):
W „stanie spoczynku” komórka mięśnia sercowego znajduje się w stanie tzw. potencjału spoczynkowego (polaryzacji), czyli przezbłonowego gradientu ładunków elektrycznych:
- potencjał spoczynkowy wynosi ok. −90 mV;
- jony sodu znajdują się w większym stężeniu na zewnątrz komórki, jony potasu w większym wewnątrz niej;
- błona komórkowa jest praktycznie nieprzepuszczalna dla jonów sodu w trakcie spoczynku (nie wnikają one do komórki drogą biernej dyfuzji zgodnie z gradientem stężeń. Przy błonie przepuszczalnej doszłoby do wyrównania stężeń po obu stronach błony i zaniku polaryzacji!);
- błona komórkowa w stanie spoczynku jest przepuszczalna dla jonów potasu, a istniejąca różnica stężeń tego jonu pomiędzy wnętrzem komórki a przestrzenią zewnątrzkomórkową kieruje siłę dyfuzji na zewnątrz, przeciwdziałając różnicy potencjału;
- różnica potencjału pomiędzy wnętrzem komórki a przestrzenią międzykomórkową utrzymywana jest enzymatycznie, aktywnie przez pompę jonową (ATPaza), która wbrew gradientowi stężeń i potencjałom ładunków elektrycznych wydala z komórki 3 jony sodu na każde 2 jony potasu wprowadzone do komórki. Ta różnica 3:2 przyczynia się do wytwarzania potencjału błonowego.
Potencjał czynnościowy[edytuj | edytuj kod]
Bodziec działający na spolaryzowaną komórkę mięśnia sercowego (prawidłowo z węzła zatokowo-przedsionkowego) zmienia przepuszczalność błony dla jonów sodu, które dostając się do wnętrza komórki, zmniejszają ujemny potencjał do wartości ok. −65 mV (potencjał progowy).
Przekroczenie potencjału progowego jest czynnikiem wyzwalającym otwarcie kanałów sodowych. Dochodzi wówczas do gwałtownego napływu jonów sodu do wnętrza komórki, w wyniku czego następuje szybka i całkowita depolaryzacja.
Przy wartości −40 mV otwierają się z lekkim opóźnieniem kanały wapniowe.
W powstającym potencjale czynnościowym wyróżniamy pięć faz:
- faza 0 (szybka depolaryzacja) – zależy od szybkiego dokomórkowego prądu sodowego,
- faza 1 (wstępna szybka repolaryzacja) – dokomórkowy prąd chlorkowy (w mięśniówce komór) i odkomórkowy prąd potasowy (w mięśniówce przedsionków),
- faza 2 (powolna repolaryzacja) – tzw. faza plateau (stabilizacja potencjału, stan równowagi pomiędzy dokomórkowym prądem wapniowo-sodowym a odkomórkowym prądem potasowym),
- faza 3 (szybka repolaryzacja) – przewaga odkomórkowego prądu potasowego nad wygasającym dokomórkowym prądem wapniowo-sodowym,
- faza 4 (polaryzacja) – faza spoczynku, polaryzacji.
Komórki rozrusznikowe serca mają zdolność do tzw. spontanicznej powolnej depolaryzacji w czwartej fazie potencjału czynnościowego.
Wpływ depolaryzacji na poszczególne odprowadzenia[edytuj | edytuj kod]

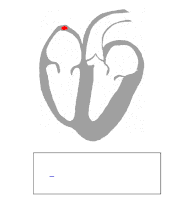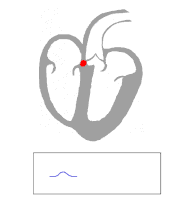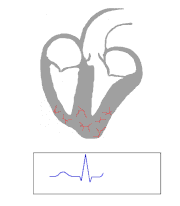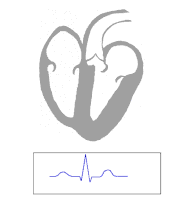
Pobudzenie elektryczne rozchodzi się (uogólniając) z prawej górnej strony serca i biegnie w kierunku dolnym i na stronę lewą. W przypadku kiedy odprowadzenie odczytuje przebieg prądu „od elektrody”, wychylenie na wykresie jest ujemne (na przykład w odprowadzeniu V1). Jeśli fala depolaryzacji biegnie w kierunku elektrody, wychylenie jest dodatnie (na przykład w odprowadzeniu V6). Jeżeli fala depolaryzacji biegnie prostopadle do elektrody wychylenie jest idiopatyczne – takie samo wychylenie w górę jak i w dół (przypadek 3 na rycinie obok).
Tkanki martwicze (na przykład objęte zawałem) inaczej przewodzą prąd niż tkanki zdrowe. Te różnice w przewodzeniu pomagają lekarzowi w ustaleniu rozpoznania.
Standardowe EKG[edytuj | edytuj kod]
Standardowe EKG wykonuje się przy pomocy 12 odprowadzeń:
- 3 dwubiegunowe kończynowe Einthovena (I, II, III),
- 3 jednobiegunowe kończynowe wzmocnione Goldbergera (aVR, aVL, aVF),
- 6 jednobiegunowych przedsercowych Wilsona (V1, V2, V3, V4, V5, V6).
Odprowadzenia dwubiegunowe kończynowe Einthovena[edytuj | edytuj kod]
W tym odprowadzeniu umieszczamy 4 elektrody na ciele badanego:
- elektroda czerwona – prawa ręka (RA),
- elektroda żółta – lewa ręka (LA),
- elektroda zielona – lewa łydka (LF),
- elektroda czarna – prawa łydka (tzw. punkt odniesienia; ziemia).
Trzy pierwsze elektrody tworzą tzw. trójkąt Einthovena, który w założeniu jest trójkątem równobocznym, co sprawia, iż linie poprowadzone prostopadle z każdego ze środków trzech boków, reprezentujące zerowy potencjał, przetną się w środku trójkąta.
Pomiędzy pierwszymi trzema ww. elektrodami wykonuje się pomiar różnicy potencjałów (w mV):
- odprowadzenie I – różnica potencjałów pomiędzy elektrodami „lewa ręka” a „prawa ręka” (LA – RA),
- odprowadzenie II – różnica potencjałów pomiędzy elektrodami „lewa łydka” a „prawa ręka” (LF – RA),
- odprowadzenie III – różnica potencjałów pomiędzy elektrodami „lewa łydka” a „lewa ręka” (LF – LA).
Odprowadzenia jednobiegunowe kończynowe wzmocnione Goldbergera[edytuj | edytuj kod]
Z powyższych 3 elektrod odczytujemy również wzmocnione (ang. augmented – wzmocniony, powiększony) sygnały:
- odprowadzenie aVR – z elektrody „prawa ręka” (RA),
- odprowadzenie aVL – z elektrody „lewa ręka” (LA),
- odprowadzenie aVF – z elektrody „lewa goleń” (LF).
Odprowadzenia jednobiegunowe przedsercowe Wilsona[edytuj | edytuj kod]

Połączenie razem 3 ww. odprowadzeń kończynowych daje teoretycznie wypadkowy potencjał równy 0. Ten wspólny punkt można połączyć z ujemnym biegunem galwanometru, a kolejne elektrody połączyć z biegunem dodatnim galwanometru.
W standardowym 12-odprowadzeniowym EKG wykorzystuje się 6 elektrod jednobiegunowych przedsercowych Wilsona:
- V1 – czerwona elektroda – w prawym czwartym międzyżebrzu (przestrzeni międzyżebrowej) przy brzegu mostka,
- V2 – żółta elektroda – w lewym czwartym międzyżebrzu (przestrzeni międzyżebrowej) przy brzegu mostka,
- V3 – zielona – w połowie odległości pomiędzy elektrodami V2 a V4,
- V4 – brązowa elektroda – w lewym piątym międzyżebrzu (przestrzeni międzyżebrowej) w linii środkowo-obojczykowej lewej,
- V5 – czarna elektroda – w lewym piątym międzyżebrzu (przestrzeni międzyżebrowej) w linii pachowej przedniej lewej,
- V6 – fioletowa elektroda – w lewym piątym międzyżebrzu (przestrzeni międzyżebrowej) w linii pachowej środkowej lewej.
Charakterystyka EKG – elektrokardiogram[edytuj | edytuj kod]

Na wykresie EKG analizuje się:
- linię izoelektryczną – linia pozioma zarejestrowana w czasie, gdy w sercu nie stwierdza się żadnych pobudzeń (aktywności). Najłatwiej wyznaczyć ją według odcinka PQ. Stanowi ona punkt odniesienia poniższych zmian;
- załamki – wychylenia od linii izoelektrycznej (dodatni, gdy wychylony w górę; ujemny, gdy wychylony w dół);
- odcinki – czas trwania linii izoelektrycznej pomiędzy załamkami;
- odstępy – łączny czas trwania odcinków i sąsiadującego załamka.
Załamki[edytuj | edytuj kod]
- załamek P – jest wyrazem depolaryzacji mięśnia przedsionków (dodatni we wszystkich 11 odprowadzeniach, poza aVR, tam ujemny)
- zespół QRS – odpowiada depolaryzacji mięśnia komór (w tym czasie następuje również repolaryzacja przedsionków, którą przysłania zespół QRS)
- załamek T – odpowiada repolaryzacji komór
- czasami też załamek U – odpowiada późnej repolaryzacji mięśni brodawkowatych
Odcinki[edytuj | edytuj kod]
- odcinek PQ – wyraża czas przewodzenia depolaryzacji przez węzeł przedsionkowo-komorowy (AV)
- odcinek ST – okres początkowej repolaryzacji mięśnia komór
Odstępy[edytuj | edytuj kod]
- odstęp PQ – wyraża czas przewodzenia depolaryzacji przez cały układ bodźcoprzewodzący serca, to jest od węzła zatokowo-przedsionkowego do włókien Purkiniego i wynikającą z tego depolaryzację przedsionków
- odstęp ST – wyraża czas wolnej i szybkiej repolaryzacji mięśnia komór (2 i 3 faza repolaryzacji)
- odstęp QT – wyraża czas potencjału czynnościowego mięśnia komór (depolaryzacja + repolaryzacja)
Szczególne fragmenty[edytuj | edytuj kod]
- zwrot ujemny – w odprowadzeniach przedsercowych fragment zespołu QRS, od początku zespołu do szczytu ostatniego załamka R
- pobudzenie istotne komór ≠ zwrot ujemny! – to fragment od początku zespołu QRS do szczytu załamka R, zwany także opóźnieniem ujemnego zwrotu
Interpretacja wyniku EKG[edytuj | edytuj kod]
Interpretacja wyniku EKG zależy od wielu czynników, z których najważniejsze to wiek, stosowane leki i schorzenia pozasercowe. Interpretacji wyniku powinien dokonać lekarz lub ratownik medyczny.
Prawidłowy i patologiczny elektrokardiogram:
- Załamek P
- Załamek P powstaje w wyniku depolaryzacji przedsionków (prawego i lewego), jego część wstępująca jest związana z przejściem fali depolaryzacyjnej przez przedsionek prawy, a zstępująca przez przedsionek lewy. Prawidłowy załamek P w odprowadzeniach I, II, aVF i V2-V6 jest dodatni, często także w odprowadzeniu III, w odprowadzeniu aVR ujemny, w odprowadzeniu aVL najczęściej płaski, w odprowadzeniu V1 dodatni, dwufazowy albo ujemny.
- Czas trwania prawidłowego załamka P jest krótszy od 0,12 s (3 mm przy zapisie 25 mm/s), amplituda nie przekracza 2,5 mm w odprowadzeniach I, II, III, aVR, aVL, aVF i 3 mm w odprowadzeniach V1-V6.
- Załamek P uznaje się za nieprawidłowy gdy zapis jest zazębiony, rozdwojony, przekraczający powyższe parametry (amplituda, czas trwania, polaryzacja w odpowiednich odprowadzeniach np. ujemny w I). Zmniejszenie się amplitudy załamka w odniesieniu do poprzedniego badania może być spowodowane obniżeniem się rozrusznika w dolną część węzła zatokowego lub poniższych ośrodków bodźcotwórczych na przestrzeni prawego przedsionka.
- Wysoka amplituda załamka P występuje przy przeroście prawego przedsionka oraz u osób ze zwiększoną aktywnością układu współczulnego.
- Szeroki, często rozdwojony załamek P świadczy o przeroście lewego przedsionka lub nieprawidłowym napływie krwi do lewej komory serca.
- Ujemna wartość amplitudy w odprowadzeniu I może świadczyć o rytmie lewego przedsionka (prawidłowy rytm pochodzi z węzła zatokowo-przedsionkowego na prawym przedsionku), nieprawidłowym położeniu serca w klatce piersiowej lub zaawansowanym przeroście prawego przedsionka.
- Ujemne wartości w odprowadzeniach II, III i aVF świadczą o wstecznej propagacji fali depolaryzacyjnej (rytm ektopowy) z dolnej części przedsionków lub węzła przedsionkowo-komorowego bądź z komór.
- Zawyżenia kształtu części wstępującej lub zstępującej lub rozdwojenie załamka świadczy o zaburzeniach przewodzenia wewnątrzprzedsionkowego.
- Niekiedy załamki P są niewidoczne. Nie są rejestrowane przy braku czynności elektrycznej przedsionków, podczas migotania przedsionków widoczne są drgania linii izoelektrycznej (fala f fibrillatio), przy trzepotaniu przedsionków drgania są wyraźne i regularne. Migotanie i trzepotanie najlepiej jest widoczne na zapisie z odprowadzeń V1, V2 oraz II. Załamek P może być ukryty w zespole QRS (wówczas rytm pochodzi z węzła przedsionkowo-komorowego) lub w załamku T poprzedniej ewolucji serca (blok przedsionkowo-komorowy I stopnia).
Zobacz też[edytuj | edytuj kod]
Linki zewnętrzne[edytuj | edytuj kod]
- ECGSIM [online], www.ecgsim.org [dostęp 2020-02-07] (ang.). Program symulacyjny demonstrujący zależność pomiędzy elektryczną aktywnością serca a wykresem EKG. Dostępny na licencji GNU GPL.
- ECG library [online], www.ecglibrary.com [dostęp 2020-02-07] (ang.).
- A (not so) brief history of electrocardiography [online], www.ecglibrary.com [dostęp 2020-02-07] (ang.).
- EKG Academy. Learn, Practice, Reference [online], Clinical Skills Education, 2016 [dostęp 2020-02-07] (ang.).
- Sekcja Elektrokardiologii Nieinwazyjnej i Telemedycy PTK [online], senit.pl [dostęp 2020-02-07].


 French
French Deutsch
Deutsch