آکلیدینیوم برومید - ویکیپدیا، دانشنامهٔ آزاد
 | |
| دادههای بالینی | |
|---|---|
| نامهای تجاری | Bretaris Genuair, Eklira Genuair, Tudorza Pressair |
| AHFS/Drugs.com | monograph |
| دادهها | |
| روش مصرف دارو | استنشاقی |
| کد ATC | |
| وضعیت قانونی | |
| وضعیت قانونی |
|
| دادههای فارماکوکینتیک | |
| زیست فراهمی | <۵٪ (سیستمی) ۳۰٪ (در ریه) |
| متابولیسم | استر هیدرولیز |
| نیمهعمر حذف | ۲–۳ ساعت |
| مدت زمان اثر | >۲۴ ساعت |
| دفع | ۶۵٪ ادرار، ۳۳٪ مدفوع |
| شناسهها | |
| |
| شمارهٔ سیایاس | |
| پابکم CID | |
| دراگبنک | |
| کماسپایدر | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| CompTox Dashboard (EPA) | |
| ECHA InfoCard | 100.260.213 |
| دادههای فیزیکی و شیمیایی | |
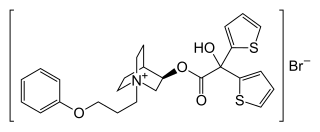
| فرمول شیمیایی | C26H30BrNO4S۲ |
| جرم مولی | ۵۶۴٫۵۵ g·mol−1 |
| مدل سه بعدی (جیمول) | |
| |
| |
| | |
آکلیدینیوم برومید (انگلیسی: Aclidinium bromide) یک آنتاگونیست موسکارینی استنشاقی طولانیاثر (LAMA) است که در ۲۴ ژوئیه ۲۰۱۲[۱] در ایالات متحده آمریکا بهعنوان درمان نگهدارنده برای بیماری انسدادی مزمن ریوی (COPD) تأیید شد.[۲]
شواهد نشان میدهد که میتواند کیفیت زندگی را بهبود بخشد و از بستری شدن در بیمارستان در مبتلایان به COPD جلوگیری کند. با این حال، به نظر نمیرسد که بر خطر مرگ یا دفعات مورد نیاز استروئیدها تأثیر بگذارد. مشخص نیست که آیا این دارو با داروهای مشابه تیوتروپیوم یا سایر داروهای رایج مورد استفاده در کلاس LAMA تفاوت دارد یا خیر.[۳]
آکلیدینیوم از راه یک استنشاق کننده پودر خشک چند دوز، استنشاقی Genuair تحویل داده میشود. این دارو در فهرست داروهای ضروری سازمان بهداشت جهانی قرار دارد.[۴]
اثرات نامطلوب[ویرایش]
این ماده بهطور کلی به خوبی تحمل میشود. عوارض جانبی شایع (در بیش از ۱ درصد بیماران) سینوزیت، نازوفارنژیت، سردرد، سرفه، اسهال و حالت تهوع است. مورد دوم تحت دارو کمتر از دارونما است.[۵] واکنشهای پوستی مانند بثورات، و همچنین عوارض جانبی معمول آنتاگونیستهای موسکارینی (ضربان قلب سریع، تپش قلب، و احتباس ادرار) در کمتر از ۱٪ از بیماران رخ میدهد.
اافزایش اندک خطر قلبی عروقی را نمیتوان از دادههای موجود مستثنی کرد. بیماران مبتلا به بیماریهای قلبی عروقی مرتبط از مطالعه حذف شدند.
تداخلات[ویرایش]
هیچ مطالعه متقابل سیستماتیک انجام نشدهاست. انتظار میرود که اثرات نامطلوب آکلیدینیوم در صورت ترکیب با سایر آنتاگونیستهای موسکارینی افزایش یابد. در عمل بالینی، هیچ تداخلی با سایر داروهای COPD مانند گلوکوکورتیکوئیدها، آگونیستهای β۲ آدرنرژیک و تئوفیلین شرح داده نشدهاست. از آنجایی که آکلیدینیوم بهطور مرتبط با آنزیمهای کبدی سیتوکروم P450 یا P-گلیکوپروتئین تعامل ندارد و به محض رسیدن به جریان خون به سرعت متابولیزه میشود، در نظر گرفته میشود که پتانسیل بسیار کمی برای تداخل و برهمکنش دارد.
فارماکولوژی[ویرایش]
مکانیسم عمل[ویرایش]
آکلیدینیوم یک آنتاگونیست طولانی اثر و برگشتپذیر در گیرندههای موسکارینی است، با میل ترکیبی مشابه با هر پنج زیرگروه، اما با نیمه عمر تفکیک از زیرگروه M3 ۲۹٫۲ ساعت یا شش برابر بیشتر از M2. برای مقایسه، نیمه عمر تجزیه M3 داروهای مرتبط ایپراتروپیوم و تیوتروپیم به ترتیب ۰٫۴۷ ساعت و ۶۲٫۲ ساعت است.
عملکرد آن در زیرگروه M3 در عضله صاف برونشیولها مسئول اثر مطلوب آن است: انقباض این ماهیچهها را کاهش میدهد و جریان هوا را بهبود میبخشد. میل M2 دلیل اصلی اثرات نامطلوب در قلب است.
فارماکوکینتیک[ویرایش]
حدود ۳۰ درصد از آکلیدینیوم استنشاقی در ریه رسوب میکند. عمل آن در آنجا بیش از ۲۴ ساعت طول میشد. از ریه، به جریان خون جذب میشود و پس از پنج دقیقه در افراد سالم و پس از ۱۰ تا ۱۵ دقیقه در بیماران COPD به بالاترین غلظت پلاسمای خون میرسد. این ماده به سرعت به اسید کربوکسیلیک و الکل هیدرولیز میشود، به طوری که کمتر از ۵٪ از دوز استنشاقی بدون تغییر در پلاسما یافت میشود. هیدرولیز هم غیر آنزیمی و هم آنزیمی است، دومی عمدتاً توسط بوتیریل کولین استراز.[۵][۶]
متابولیت اسید دارای اتصال پروتئین پلاسما ۸۷٪ و الکل ۱۵٪ است. این متابولیتها تا ۶۵ درصد در ادرار و ۳۳ درصد در مدفوع یافت میشوند. نیمه عمر حذف دو تا سه ساعت است. آکلیدینیوم بدون تغییر تنها ۰٫۱ درصد از دوز دفع شده را تشکیل میدهد.
منابع[ویرایش]
- ↑ "Forest Laboratories and Almirall Announce FDA Approval of Tudorza Pressair for the Long-Term Maintenance Treatment of COPD" (Press release). Forest Laboratories. Retrieved 2012-07-24.
- ↑ Gavaldà A, Miralpeix M, Ramos I, et al. (2009). "Characterization of aclidinium bromide, a novel inhaled muscarinic antagonist, with long duration of action and a favorable pharmacological profile". J Pharmacol Exp Ther. 331 (2): 740–51. doi:10.1124/jpet.109.151639. PMID 19710368. S2CID 10533142.
- ↑ Ni, H; Soe, Z; Moe, S (2014). "Aclidinium bromide for stable chronic obstructive pulmonary disease". The Cochrane Database of Systematic Reviews (9): CD010509. doi:10.1002/14651858.CD010509.pub2. PMID 25234126.
- ↑ World Health Organization (2021). World Health Organization model list of essential medicines: 22nd list (2021). Geneva: World Health Organization. hdl:10665/345533. WHO/MHP/HPS/EML/2021.02.
- ↑ ۵٫۰ ۵٫۱ Haberfeld, H, ed. (2015). Austria-Codex (به آلمانی). Vienna: Österreichischer Apothekerverlag.
- ↑ Dinnendahl, V; Fricke, U, eds. (2014). Arzneistoff-Profile (به آلمانی). Vol. 1 (27 ed.). Eschborn, Germany: Govi Pharmazeutischer Verlag. ISBN 978-3-7741-9846-3.
پیوند به بیرون[ویرایش]
| در ویکیانبار پروندههایی دربارهٔ آکلیدینیوم برومید موجود است. |


 French
French Deutsch
Deutsch