Ecodoppler venoso dos membros inferiores – Wikipédia, a enciclopédia livre

O ecodoppler venoso dos membros inferiores é um exame não invasivo que utiliza os ultrassons de modo a adquirir informações sobre a anatomia, fisiologia e a patologia do sistema venoso superficial e profundo.[1]
Está indicado principalmente no estudo de duas patologias: trombose venosa e insuficiência venosa. À semelhança da ecocardiografia, a ultrassonografia venosa requer uma compreensão de hemodinâmica de modo a fornecer relatórios de exame fiáveis e úteis. Na insuficiência venosa, o exame ecodoppler é extremamente útil na confirmação da doença varicosa, ao fazer uma avaliação da hemodinâmica, avaliando a progressão da doença e a sua resposta ao tratamento. Tornou-se a referência standard para o estudo dessa patologia.[2]
Desde a sua introdução nos anos 60,[3] os ultrassons foram rapidamente aplicados à medicina, contribuindo enormemente para a precisão e rapidez do diagnóstico e do tratamento subsequente. Fácil de executar, mas difícil de interpretar, a ecografia, posteriormente associada à codificação a cores e ao efeito Doppler, veio revolucionar o mundo da imagiologia, da obstetrícia, da cardiologia, da angiologia entre outros. Porém, a sua execução requer um treino adequado para que não se caia em erros de diagnóstico.[4] Na verdade, os conhecimentos e o treino do examinador são tanto ou mais importantes que o equipamento propriamente dito. Se a ecografia está relacionada com o estudo da imagem na maioria das disciplinas, já a sua aplicação ao estudo das veias não é linear e um conhecimento aprofundado de hemodinâmica é absolutamente necessário para que o examinador forneça um exame de qualidade e útil ao posterior tratamento do paciente.[5] A dificuldade deste exame e a falta de centros especializados para ministrar o treino necessário fazem com que ainda hoje os resultados do exame sejam controversos.[6]
É um exame inócuo, o paciente não é exposto a radiações, pode ser usado em qualquer idade, não necessita de preparação (salvo para estudar os eixos venosos abdominais), tem índices de sensibilidade e especificidade de cerca de 90% respetivamente e apesar do custo do material, é considerado como um exame pouco dispendioso e de primeira linha para a confirmação de um diagnóstico.[4][7]
A importância deste exame, no caso do estudo da insuficiência venosa crónica, não se limita a confirmar que esta insuficiência existe. Sendo um exame predominantemente hemodinâmico e dado o desenvolvimento que tem sido feito no campo do tratamento das varizes, este exame deve fornecer indicações ao cirurgião sobre as possibilidades de restabelecer a drenagem do sistema venoso superficial. É indispensável a exatidão destas informações e a elaboração de uma cartografia detalhada quando está previsto efetuar um tratamento conservador. Sobre esta cartografia o hemodinamista que efetuou o exame, em equipa com o cirurgião, marcará os pontos essenciais para que a correção cirúrgica seja efetuada(dissecção virtual).[nota 1][8]
Princípios básicos da ultrassonografia[editar | editar código-fonte]
A ultrassonografia baseia-se no princípio de que o som pode passar através dos tecidos do corpo humano e ser reflectido pelas interfaces tissulares[nota 2] do mesmo modo que a luz pode reflectir-se num espelho. Os tecidos oferecem vários graus de resistência, conhecida como impedância acústica, à passagem do feixe de ultrassons. Quando há uma agrande diferença de impedância entre dois planos tissulares, a interface entr eles reflectirá fortemente o som. Quando o feixe de ultrassons encontra o ar, ou um tecido sólido como o osso, a diferença de inpedância é tão grande que a maioria da energia acústica é reflectida tornando impossível ver as estruturas que estão para lá dessa barreira. O examinador verá só uma sombra, em vez da imagem prevista. Esta é também a razão pela qual se coloca um gel entre a sonda e a pele para evitar que haja ar a impedir a correta visualização. Os líquidos, incluindo o sangue, têm uma baixa impedância, o que significa que pouca energia será reflectida e a visualização não é possível. Porém, quando o fluxo sanguíneo é muito lento pode ser visualizado, o que é chamado de "contraste espontâneo".[9][10][11]

Esta tecnologia é largamente utilizada para confirmar os diagnósticos em patologia venosa. A qualidade de imagem necessária tornou-se possível com o desenvolvimento do Doppler. O desenvolvimento da técnica doppler conduziu à introdução da cor permitindo "visualizar" o fluxo sanguíneo num determinado sector da imagem e ter informações sobre a direção e velocidade desse mesmo fluxo. Trata-se de uma informação codificada na qual, por convenção, o fluxo que se dirige para a sonda aparece a vermelho e o fluxo que se afasta da sonda aparece a azul. Esta disposição de cores pode ser invertida e a gama de cores pode ser modificada no aparelho; seja como for, no ecrã aparecerá um retângulo vertical com as cores escolhidas no qual a superior será a cor do fluxo que se dirige para a sonda. Uma coloração uniforme do fluxo significa que estamos em presença de um fluxo laminar.[nota 3] No caso de existirem turbulências, várias colorações aparecerão, misturando amarelo,vermelho,verde e branco. Mudando sucessivamente o sector visualizado podemos adquirir uma informação importante sobre a velocidade, direção e características (laminar ou turbulento) do fluxo sanguíneo num determinado vaso.[9][10][11]
Diferentes sondas são necessárias de acordo com a profundidade dos tecidos que desejamos estudar. O treino e a experiência do examinador são extremamente importantes devido aos muitos problemas técnicos. A anatomia venosa, por exemplo não é constante, varia de pessoa para pessoa, e na mesma pessoa a disposição venoso do membro inferior direito não é igual à do esquerdo.[5][12][13]
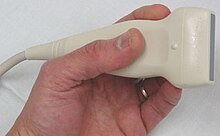
A sonda é um sensor ultrassónico, geralmente conhecido por transdutor, que funciona enviando e recebendo a energia acústica. É um emissor/receptor de ultrassons e consoante o tipo de sonda assim os ultrassons emitidos vão atingir uma profundidade maior ou menor. Quanto mais alta a frequência, menor a profundidade atingida e vice-versa. A emissão de ultrassons gera-se nos cristais da sonda pelo efeito piezoeléctrico. Os ultrassons são recebidos pela sonda, transformados em impulso eléctrico, voltagem, e enviados ao aparelho para processamento do sinal e conversão em imagem no ecrã. A profundidade atingida pelo feixe de ultrassons é dependante da frequência da sonda usada. Quanto maior a frequência, menor será a profundidade atingida.[14]
Material utilizado[editar | editar código-fonte]
Este exame necessita de um aparelho de ultrassonografia de alta qualidade para que tenha a capacidade de um correto tratamento de imagem. Deverá poder ser capaz de fornecer uma informação de excelente qualidade sobretudo nos planos mais superficiais, efetuar Doppler de emissão pulsada e codificação a cores. As sondas utilizadas dependem da profundidade a ser estudada; assim, para o sistema venoso superficial usa-se uma sonda linear[nota 4] de 12 MHz, no caso de pacientes com tecido adiposo mais espesso uma sonda de 7.5 MHz é preferível. Para o sistema venoso profundo acima do nível inguinal, veias ilíacas e veia cava inferior, uma sonda sectorial de 4 a 6 MHz será necessária. Assim, é preciso três sondas e uma máquina de boa qualidade, o que equivale a dizer que este tipo de material é oneroso. Por outro lado a experiência do examinador é fundamental e condiciona os resultados do exame. Ao contrário do estudo arterial, a estrutura da parede venosa tem pouca importância e o fundamental são as ilações hemodinâmicas que o exame deve fornecer.[15] Deste modo, a formação do examinador em hemodinâmica é primordial, sem a qual este exame perderá todo o seu valor.[5][16]

Importância e indicações[editar | editar código-fonte]
A finalidade deste exame incide principalmente sobre o estudo de duas patologias distintas, a insuficiência venosa superficial e/ou profunda e a trombose venosa também superficial e/ou profunda.[17]
Permite ao examinador estudar a anatomia do do sistema venoso superficial e profundo assim como a direção do fluxo sanguíneo, o qual é crucial na determinação da patologia venosa. Tornou-se o exame de referência usado na avaliação da situação e hemodinâmica da patologia venosa dos membros inferiores.[2]
O fluxo sanguíneo normal, fisiológico, nas veias é anterógrado[nota 5], de modo que a evidência do oposto, fluxo retrógrado, pode significar patologia venosa. A presença de um refluxo é também importante; quando não é isolado numa veia (no caso de um fluxo retrógrado), significa que o fluxo sanguíneo é bi-direccional onde deveria ser anterógrado.[18][19]
Este exame não deve ser efetuado sem indicação médica ou cirúrgica, tal como a suspeita de uma trombose venosa[20] [21]ou o estudo da doença varicosa. Está a ser efetuado como rotina e em alguns hospitais, no post-operatório ortopédico nomeadamente na cirurgia do joelho. A justificação para tal rotina nestas condições explica-se pela presença de edema e dor secundários à cirurgia que podem mascarar a presença de uma trombose venosa profunda.[22]
Técnica de exame[editar | editar código-fonte]
No caso de suspeita de trombose venosa superficial ou de trombose venosa profunda, este exame pode ser efectuado com o paciente deitado, já no caso do estudo da insuficiência venosa ele deve ser executado obrigatoriamente em posição de pé (ortostatismo). Esta posição permite o estudo da competência valvular e da direção do fluxo sanguíneo.[23]
O protocolo de exame varia consoante o fim a que se destina o estudo. Assim, o protocolo utilizado para um estudo das alterações hemodinâmicas num paciente com insuficiência venosa é muito diferente do protocolo de investigação de uma suspeita de trombose venosa. O exame efetuado com a intenção de tratar o paciente por stripping ou terapia por laser, por exemplo, é muito diferente do exame executado com a intenção de efetuar uma Cura CHIVA.[24][25]
Trombose venosa[editar | editar código-fonte]
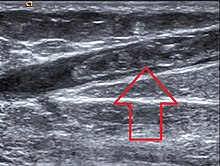
Ao contrário do ecodoppler arterial, no ecodoppler venoso a sonda deve estar perpendicular ao eixo do vaso, logo, nas imagens adquiridas, as veias aparecem como pequenos círculos. A razão pela qual a sonda deve estar perpendicular ao eixo do vaso[26]é que, trabalhando dessa maneira, detectam-se melhor todas as veias e suas ramificações assim como as perfurantes, o que é importantíssimo no estudo das varizes. Além disso, quando em presença de uma trombose venosa, é possível testar a compressibilidade da veia. Se a sonda estiver no sentido do eixo do vaso é fácil acontecer um pequeno deslizamento ao comprimir a veia e sair assim do plano de estudo, dando um falso negativo de trombose pois o vaso desapareceu, parecendo compressível. A falta de compressibilidade é um dos sinais mais fidedignos de trombose de uma veia[20] [27] já que um coágulo muito recente pode ser pouco visível devido à sua baixa ecogenicidade, mesmo com bons aparelhos e a codificação a cores pode originar um falso negativo ou um falso positivo. Não ver o coágulo não significa que ele não exista, não ver com nitidez o lúmen da veia não significa presença de coágulo.[20] A localização e o aspecto do trombo determina a gravidade da situação: assim deve ser sempre pesquisada a hipótese de um coágulo flutuante, sobretudo quando este coágulo se situa na junção safeno-femoral em cujo caso há uma indicação cirúrgica de urgência, pois a frequência de fragmentaçao da cabeça do coágulo e a embolia pulmonar mortal é importante.[28] [4] Em urgência existe uma técnica simplificada chamada "ecografia de compressão" que é usada para o diagnóstico rápido da trombose venosa profunda, principalmente a nível da veia femoral comum e veia poplítea. Este exame abreviado é extremamente útil e é efetuado pela simples compressão das veias com a sonda.[29]
A ecogradia de compressão tem uma alta sensibilidade/especificidade nos pacientes sintomáticos. Os resultados não são fiáveis quando o paciente é assintomático. Por exemplo, no pós-operatório de alto risco, sobretudo em cirurgia ortopédica, cujos pacientes já têm dor e edema, um exame cuidadoso e exaustivo é obrigatório.[30][31][32]
Insuficiência venosa superficial[editar | editar código-fonte]
Quando se estuda a insuficiência venosa superficial, a visualização da parede da veia tem pouca importância e toda a atenção deve ser centrada na direcção do fluxo sanguíneo. O objetivo deste exame é estudar como as veias drenam. Trata-se portanto, de um exame de hemodinâmica e não um exame de pura imagiologia. O estudo das varizes é assim reservado aos especialistas com formação aprofundada em hemodinâmica e o treino adequado em ecodoppler.[16]
Mais uma vez, ao contrário do que acontece com o ecodoppler arterial, a velocidade do sangue nas veias não tem qualquer implicação diagnóstica. As veias são um sistema de drenagem, o equivalente de um sistema hidráulico de baixa pressão, com um fluxo laminar e lento. Esta lentidão faz com que a sua velocidade só seja detectada espontaneamente pelo efeito Doppler nas veias de maior calibre como as veias ilíacas e femorais.Nestas veias o fluxo venoso é modulado pela respiração ou é contínuo no caso de haver alto débito. As veias de menor diâmetro não mostram fluxo espontâneo de modo que para visualizar a direção do fluxo venoso é necessário aumentar a velocidade deste fluxo utilizando manobras, usualmente de compressão e descompressão, a manobra de Valsalva e a manobra de Paraná. A velocidade conseguida dependerá da eficácia do examinador ao efetuar a compressão e descompressão ou a manobra de Paraná, e da capacidade do paciente para executar corretamente a manobra de Valsalva.[33]
Em casos de estase venosa, o lúmen da veia aparece no monitor como que preenchido por material ecógeno[nota 6], que não é mais do que o sangue visualizado e a que se chama "contraste espontâneo". Esta imagem pode ser confundida com um trombo. Porém a veia é facilmente compressível e à descompressão aparece a imagem clássica da veia com o interior completamente negro ou cinzento escuro, como é habitual.[33]
Toda a concentração do examinador incidirá principalmente sobre a direção do fluxo sanguíneo na rede venosa profunda, nos troncos principais superficiais (veia grande safena e safena externa ou pequena safena), nas suas colaterais, assim como no estado funcional das veias perfurantes, e na presença ou ausência de shunts.[nota 7][5][34]
Para complicar ainda mais a execução do exame, este deve ser efetuado como se disse acima com a sonda em posição transversal em relação ao eixo do vaso mas a cartografia será desenhada no sentido longitudinal o que obriga a uma rápida extrapolação, na mente do examinador, do sentido transversal para o longitudinal o que nem sempre é evidente para quem efetua o exame.[34]
 |  |  |  |
Dificuldades técnicas[editar | editar código-fonte]
O ecodoppler venoso é um dos exames complementares de diagnóstico, realizados por médicos ou técnicos especializados para o efeito, em que a competência do examinador mais influencia os resultados. Não só a execução não é fácil, mas também a interpretação dos resultados é subjetiva e proporcional aos conhecimentos do examinador em hemodinâmica venosa. A técnica de execução é completamente diferente da utilizada para fazer um ecodoppler arterial.[5][12]
A situação complica-se ainda mais na medida em que existem veias sem dilatação mas insuficientes; veias que podem ser insuficientes durante o Verão, com o calor, e serem perfeitamente continentes durante o Inverno; veias dilatadas, sem insuficiência, só porque debitam demais (é o caso da pequena safena quando é chamada a ajudar na drenagem do território da grande safena no caso de oclusão ou grave insuficiência desta última veia).[5]
Outra dificuldade é que a anatomia venosa superficial não é constante, apresenta muitas variantes anatómicas e no mesmo paciente usualmente o membro inferior direito é anatomicamente diferente do esquerdo. As veias não estão onde são procuradas, mas sim onde são encontradas. A execução das manobras dinâmicas para efetuar este exame também pode se fonte de dificuldade de execução para os examinadores menos experientes.[13]
Principais veias superficiais estudadas[editar | editar código-fonte]
Grande safena[editar | editar código-fonte]

A grande safena ou safena interna, origina-se pela confluência das veias do pé e individualiza-se a nível da face antero-interna do tornozelo imediatamente à frente do maléolo interno. Sobe na face antero-interna da perna e da coxa, recebendo inúmeros ramos colaterais e drenando nas veias profundas por múltiplas perfurantes até se jogar na veia femoral comum a nível da região inguinal ou virilha. No seu trajeto está situada num desdobramento entre a fascia superficial e a fascia profunda que os anatomistas consideram hoje um compartimento, chamado o compartimento safeniano.[35] ao ser visualisado em ecografia e em corte transversal este compartimento apresenta uma forma característica lembrando um olho, com as duas pálpebras e a íris que é a imagem da safena. Chama-se em ecografia venosa o "Sinal do Olho".[5] Desta forma se distinguem as veias que são superficiais à fascia como veias inter-tegumentares e tributárias dos eixos safenianos e as veias que estão abaixo do folheto profundo da fascia como veias profundas. Todas as veias que tendo origem numa veia superficial, perfuram a fascia profunda e se reúnem ao sistema venoso profundo são chamadas veias perfurantes. É assim possível reconhecer ecograficamente três compartimentos anatómicos:
- profundo ou N1 (terminologia em inglês "Network") originalmente chamado de R1 (terminologia francesa, "Réseau") que contém o sistema venoso profundo
- safeniano ou N2 com as safenas mas também a veia de Giacomini e a veia safena acessória anterior antigamente chamada veia anterior da coxa
- superficial N3 que contém as veias tributárias das safenas, das quais uma a nível da face interna da perna está presente com frequência, a chamada veia do arco posterior ou veia de Leonardo (esta veia está muitas vezes insuficiente nos pacientes com varizes)
- um compartimento N4 que contém colaterais que reúnem a mesma safena em dois pontos distintos N4L (longitudinal) ou reúnem as duas safenas N4T (transversal)[5]

Esta diferenciação dos compartimentos é muito útil quando se estuda o paciente portador de insuficiência venosa pois facilita a sistematização, a criação da cartografia e posteriormente a atitude cirúrgica a tomar se tal for necessário. Pela proteção conferida pelas fascias, e pela presença de uma dupla camada muscular, as veias que pertencem ao compartimento N2 muito raramente se apresentam como varizes sinuosas e no exame físico do paciente podemos dizer que uma veia tortuosa e dilatada é uma colateral e não uma safena, com escassas probabilidades de erro.
No que se refere à safena acessória anterior, ela distingue-se ecograficamente da safena interna pelo seu trajeto mais anterior, no alinhamento dos vasos femorais ou num plano exterior a eles , enquanto que a safena interna tem um trajecto mais interno em relação a esses mesmos vasos.

Sob o ponto de vista hemodinâmico o fluxo sanguíneo é centrípeto ou anterógrado (em direção ao coração), sendo no sistema venoso superficial também da superfície para a profundidade, por intermédio das veias perfurantes. Há no entanto duas excepções: a nível da planta do pé onde cerca de 10% do fluxo vai para as veias dorsais e portanto flui da profundidade para a superfície. A outra excepção são as colaterais da junção safeno-femural que drenam do abdómen para a grande safena (cujo fluxo é responsável por inúmeros falsos positivos quando se estuda a drenagem da crossa da grande safena).[5]
No estudo da crossa da grande safena é muito útil muito aconselhável utilizar a codificação a cores juntamente com o efeito Doppler antes, durante e após a manobra de Valsalva.
As colaterais da grande safena serão testadas para verificação da direção do fluxo sanguíneo com a ajuda de manobras de compressão/descompressão.
A pequena safena[editar | editar código-fonte]
A pequena safena ou safena externa (SE), percorre a face posterior da perna até à região poplítea onde habitualmente drena na veia poplítea. As anomalias de drenagem desta veia são inúmeras. Assim, a pequena safena pode não ter conexão com a poplítea e continuar-se pela veia de Giacomini até esta drenar na grande safena a nível do 1/3 superior ou médio da coxa, drenar na poplítea por um tronco comum com a veia gemelar interna, drenar diretamente na grande safena a nível do 1/3 inferior da coxa, drenar por uma perfurante numa veia profunda do 1/3 inferior da face posterior da coxa. As imagens mostram a veia SE que vai drenar numa das veias do músculo semi-membranoso. A pesquisa de insuficiência ostial faz-se pelas manobras de compressão/descompressão. Em caso de dúvida a manobra de Paraná é a manobra de eleição neste caso. Os falsos positivos são sobretudo devidos ao registo do fluxo do tronco das veias gemelares que pode estar muito próximo do ponto de drenagem da pequena safena.[5]
 |  |  |
A veia de Giacomini[editar | editar código-fonte]
A veia de Giacomini funciona como uma comunicante entre a grande safena e a pequena safena. Normalmente a direção o seu fluxo é de baixo para cima, (sentido anterógrado) da pequena safena para a grande. Pode no entanto ser um fluxo retrógrado em caso de patologia da safena interna, como trombose ou insuficiência, em cujo caso a veia desvia o sangue para a pequena safena, a qual vai drenar parte do fluxo da grade safena na veia poplítea. É assim importantíssimo referir qual o sentido do fluxo na veia de Giacomini pois tem implicações no tratamento do paciente portador de insuficiência venosa.[36][37]
Relatório do exame[editar | editar código-fonte]
O relatório deve preencher algumas alíneas extremamente importantes:
- o estado do sistema venoso profundo, permeabilidade, compressibilidade, continência;
- se existe má drenagem ou insuficiência superficial e em que veias e/ou segmentos;
- qual a rede venosa patológica nomeadamente as colaterais e as perfurantes incontinentes;
- a presença de shunts;
- se possível, como restabelecer a drenagem, mencionando quais as perfurantes funcionantes que permitem uma drenagem correta para o sistema venoso profundo, isto em vista de uma cirurgia conservadora do sistema venoso superficial.[34]
Histórico[editar | editar código-fonte]
O efeito Doppler foi descrito pela primeira vez por Christian Doppler em 1843. Cerca de quarenta anos mais tarde, em 1880, o efeito piezoelétrico foi descoberto e confirmado por Pierre e Jacques Curie. Estas descobertas foram usadas no desenvolvimento da ultrassonografia. George Ludwig usou pela primeira vez os ultrassons com fins médicos nos fins dos anos 40.[38][39]
A utilisação da ultrassonografia em medicina se seguiu em diferentes pontos do mundo. Nos meados dos anos 50 mais investigação foi feita em Glasgow pelo Professor Ian Donald e colaboradores, que desenvolveram a tecnologia e aplicação dos ultrassons. Em 1963, em França, L. Pourcelot iniciou a sua tese que foi apresentada em 1964, e usou o Doppler pulsado para o estudo da circulação do sangue.[40] Estes estudos foram continuados por Peronneau em 1969. Dr. Gene Strandness e o grupo de bio-engenharia da Universidade de Washington, que conduziam a investigação do Doppler como uma ferramenta de diagnóstico para as doenças vasculares, publicaram o seu primeiro trabalho em 1967.[41][42]
O primeiro trabalho sobre o sistema venoso apareceu nos anos 1967-1968.[43] Os primeiros aparelhos comercialmente disponíveis datam de 1960. Depressa mais avanços na electrónica e nos materiais piezoeléctricos conduziram a uma utilização cada vez mais eficaz dos ultrassons em medicina, com possibilidades de diagnóstico cada vez mais preciso com o subsequente tratamento cada vez mais adequado. Isto teve um enorme impacto em diversas especialidades médicas e cirúrgicas, incluindo radiologia, ginecologia, obstetrícia, cardiologia e angiologia.[44][45] Rápidos avanços técnicos levaram a uma boa sensibilidade-especificidade da técnica.[46][47]
Os estudos visavam quase sempre a trombose venosa e foi a partir do aparecimento do Doppler pulsado e dos estudos de Claude Franceschi, inventor da Cura CHIVA que a insuficiência venosa crónica começa a ser realmente estudada.[34] A partir de 1990 com a codificação a cores do Doppler este exame triunfa no diagnóstico da patologia venosa e afasta definitivamente o uso da flebografia.[48] No entanto, se a codificação a cores é de grande utilidade no estudo das artérias, já no estudo das veias a sua utilidade é menos importante, com algumas exceções, podendo mesmo levar a falsos positivos ou falsos negativos.
Bibliografia[editar | editar código-fonte]
- Cobbold, Richard S. C. (2007). Foundations of Biomedical Ultrasound. Nova York: Oxford University Press. pp. 422–423. ISBN 978-0-19-516831-0
- Dauzat M.; Larroche J. P., Bray J.-M., Deklunder G., Couture A., Cesari J.-B.,Barral F. (1991). "Ultrasonographie vasculaire diagnostique". Paris: Vigot. pp. 386–437. ISBN 2-7114-1104-4
- Franceschi,C (1988). Théorie et Pratique de la Cure Conservatrice et Hémodynamique de l'Insuffisance Veineuse en Ambulatoire 1 ed. Précy-sous-Thil: Armançon. ISBN 2-906594-06-7
- Zamboni, P., Franceschi,C (2009). Principles of Venous Hemodynamics. New York: Nova Science Publishers, Inc. ISBN 978-1-60692-485-3
- «TRAINING IN DIAGNOSTICULTRASOUND: ESSENTIALS, PRINCIPLES AND STANDARDS» (PDF)
Notas
- ↑ A dissecção virtual é um esquema no papel, funcionando como projeto da cirurgia a efetuar.
- ↑ Interface é a superfície em que se passa de um tecido a outro com diferente densidade; por exemplo entre a pelo e a gordura, entre esta e a aponevrose, entre esta e o músculo.
- ↑ O fluxo é chamado de laminar quando a velocidade média se aproxima da velocidade máxima. A variância é pequena. Quando múltiplas velocidades estão presentes, com grande variância, estamos em presença de um fluxo turbulento
- ↑ Sonda linear é aquela em que os feixes de ultrassons são paralelos e mantém-se assim durante todo o seu percurso.
- ↑ Fluxo anterógrado é todo o fluxo venoso que se dirige da periferia para o coração, que é o sentido fisiológico.
- ↑ Ecógeno é todo o material que reflete os ultrassons, provocando um eco e sendo visualizado no monitor.
- ↑ Shunt é a situação na qual o sangue circula de uma veia para outra (ponto de fuga) e desta última para a primeira (ponto de re-entrada); é uma circulação em círculo vicioso.
Referências
- ↑ SVU 2011.
- ↑ a b Coleridge-Smith, P.; Labropoulos, N.; Partsch, H.; Myers, K.; Nicolaides, A.; Cavezzi, A. (2006). «Duplex Ultrasound Investigation of the Veins in Chronic Venous Disease of the Lower Limbs—UIP Consensus Document. Part I. Basic Principles». European Journal of Vascular and Endovascular Surgery. 31 (1): 83–92. PMID 16226898. doi:10.1016/j.ejvs.2005.07.019
- ↑ descotes J., Pourcelot, L. (1965). «Effet Doppler et mesure du débit sanguin». C.R.Acad.Sc.Paris (261): 253–6
- ↑ a b c WHO, p. 1-2.
- ↑ a b c d e f g h i j Zamboni, P., Franceschi,C (2009). Principles of Venous Hemodynamics. New York: Nova Science Publishers, Inc. ISBN 978-1-60692-485-3
- ↑ WHO, p. 7.
- ↑ «Normatização dos equipamentos e das técnicas para a realização de exames de ultra-sonografia vascular». Consultado em 5 de fevereiro de 2013
- ↑ Galeandro, A. I&all. «Doppler ultrasound venous mapping of the lower limbs». Consultado em 26 de janeiro de 2013
- ↑ a b Goldman 2003.
- ↑ a b Dauzat 1991, pp. 3-7.
- ↑ a b Cobbold, Richard S. C. (2007). Foundations of Biomedical Ultrasound. Nova York: Oxford University Press. pp. 422–423. ISBN 978-0-19-516831-0
- ↑ a b Rollo,H.A; Saliba O.A. «Métodos de diagnóstico não invasivos para avaliação da insuficiência venosa dos membros inferiores» (PDF). Consultado em 27 de janeiro de 2013
- ↑ a b WHO, p. 14.
- ↑ Markowitz, Joshua (2011). «Probe Selection, Machine Controls, and Equipment» (PDF). In: Carmody, Kristin; Moore, Christopher; Feller-Kopman, David. Handbook of Critical Care and Emergency Ultrasound. [S.l.: s.n.] pp. 25–38. ISBN 978-0-07-160490-1
- ↑ «Training in diagnostic ultrasound: Essentials, principles and standards. Report of a WHO Study Group». World Health Organization technical report series. 875: i–46; back cover. 1998. PMID 9659004
- ↑ a b Cina A; Bonomo L & all. «Color-Doppler sonography in chronic venous insufficiency: what the radiologist should know»
- ↑ WHO, p. 51-52.
- ↑ Labropoulos et al. 2003.
- ↑ Franceschi & Zamboni 2009, p. 25.
- ↑ a b c Dauzat M.; Larroche J. P., Bray J.-M., Deklunder G., Couture A., Cesari J.-B.,Barral F. (1991). "Ultrasonographie vasculaire diagnostique". Paris: Vigot. pp. 386–437. ISBN 2-7114-1104-4
- ↑ WHO, p. 26.
- ↑
- Members of 2007 and 2011 AAOS Guideline Development Work Groups on PE/VTED Prophylaxis; Mont, M; Jacobs, J; Lieberman, J; Parvizi, J; Lachiewicz, P; Johanson, N; Watters, W (18 de abril de 2012). «Preventing venous thromboembolic disease in patients undergoing elective total hip and knee arthroplasty.». The Journal of bone and joint surgery. American volume. 94 (8): 673–4. PMC 3326687
 . PMID 22517384. doi:10.2106/JBJS.9408edit
. PMID 22517384. doi:10.2106/JBJS.9408edit
- Members of 2007 and 2011 AAOS Guideline Development Work Groups on PE/VTED Prophylaxis; Mont, M; Jacobs, J; Lieberman, J; Parvizi, J; Lachiewicz, P; Johanson, N; Watters, W (18 de abril de 2012). «Preventing venous thromboembolic disease in patients undergoing elective total hip and knee arthroplasty.». The Journal of bone and joint surgery. American volume. 94 (8): 673–4. PMC 3326687
- ↑ Franceschi p.86.
- ↑ Mowatt-Larssen, Eric; Shortell, Cynthia K. (2012). «Treatment of Primary Varicose Veins Has Changed with the Introduction of New Techniques». Seminars in Vascular Surgery. 25 (1): 18–24. PMID 22595477. doi:10.1053/j.semvascsurg.2012.02.002
- ↑ Mowatt-Larssen, Eric; Shortell, Cynthia (2010). «CHIVA». Seminars in Vascular Surgery. 23 (2): 118–22. PMID 20685567. doi:10.1053/j.semvascsurg.2010.01.008
- ↑ ColeridgeSmith et al. 2006.
- ↑ Raghavendra 1986, pp. 89-95.
- ↑ Lastória, S., Sobreira, M.L. «Tromboflebite superficial: epidemiologia, fisiopatologia, diagnóstico e tratamento» (PDF). Consultado em 27 de janeiro de 2013
- ↑ Cogo, Alberto; Lensing, AW; Prandoni, P; Hirsh, J (1993). «Distribution of Thrombosis in Patients with Symptomatic Deep Vein Thrombosis: Implications for Simplifying the Diagnostic Process with Compression Ultrasound». Archives of Internal Medicine. 153 (24): 2777–80. PMID 8257253. doi:10.1001/archinte.1993.00410240085010
- ↑ Hollyoak, Maureen; Woodruff, Peter; Muller, Michael; Daunt, Nicholas; Weir, Paula (2001). «Deep venous thrombosis in postoperative vascular surgical patients: A frequent finding without prophylaxis». Journal of Vascular Surgery. 34 (4): 656–60. PMID 11668320. doi:10.1067/mva.2001.116803
- ↑ Elliott, C. Gregory (2000). «The Diagnostic Approach to Deep Venous Thrombosis: Diagnostic Tests for Deep Vein Thrombosis». Seminars in Respiratory and Critical Care Medicine. 21 (6): 495–504. doi:10.1055/s-2000-13187
- ↑ Jongbloets, L.M.M.; Koopman, M.M.W.; Büller, H.R.; Ten Cate, J.W.; Lensing, A.W.A. (1994). «Limitations of compression ultrasound for the detection of symptomless postoperative deep vein thrombosis». The Lancet. 343 (8906): 1142–4. PMID 7910237. doi:10.1016/S0140-6736(94)90240-2
- ↑ a b Franceschi, p. 84-85.
- ↑ a b c d Franceschi,C (1988). Théorie et Pratique de la Cure Conservatrice et Hémodynamique de l'Insuffisance Veineuse en Ambulatoire 1 ed. Précy-sous-Thil: Armançon. ISBN 2-906594-06-7
- ↑ Ricci S., Caggiati A. (dezembro de 1997). «The long saphenous vein compartment». Phlebology: 107-111
- ↑ Matas, Escribano, J. M.; Juan J, & all. «Haemodynamic strategy for treatment of diastolic anterograde giacomini varicose veins». Consultado em 26 de janeiro de 2013
- ↑ Pourandokht Khodabakhsh, Konstantinos T. Delis; Alison L. Knaggs (Dezembro de 2004). «Prevalence, anatomic patterns, valvular competence, and clinical significance of the Giacomini vein». Journal of Vascular Surgery. 40 (6): 1174–1183. doi:10.1016/j.jvs.2004.09.019. Consultado em 16 de fevereiro de 2003
- ↑ «History of the AIUM». Consultado em 24 de fevereiro de 2013. Cópia arquivada em 3 de novembro de 2005
- ↑ «The History of Ultrasound: A collection of recollections, articles, interviews and images». www.obgyn.net. Consultado em 24 de fevereiro de 2013. Arquivado do original em 5 de agosto de 2006
- ↑ Descotes J., Pourcelot, L. (1965). «Effet Doppler et mesure du débit sanguin». C.R.Acad.Sc.Paris (261): 253–6
- ↑ Zierler, R. Eugene (1 de novembro de 2002). «D. Eugene Strandness, Jr, MD, 1928–2002». Journal of Ultrasound in Medicine. 21 (11): 1323–5. Consultado em 8 de setembro de 2017. Arquivado do original em 23 de outubro de 2015
- ↑
- ↑ Feigl P., Sigel B. (1968). «A Doppler Ultrasound method for diagnosing lower extremity venous disease». Surgery, Gynecology & Obstetrics (127): 339-350
- ↑ Eyer, M.K.; Brandestini, M.A.; Phillips, D.J.; Baker, D.W. (1981). «Color digital echo/doppler image presentation». Ultrasound in Medicine & Biology. 7. 21 páginas. doi:10.1016/0301-5629(81)90019-3
- ↑ Persson, AV; Jones, C; Zide, R; Jewell, ER (1989). «Use of the triplex scanner in diagnosis of deep venous thrombosis». Archives of surgery. 124 (5): 593–6. PMID 2653279. doi:10.1001/archsurg.1989.01410050083017
- ↑ Dauzat M., Laroche J. P. (1983). «L'echotomographie des veines: proposition d'une méthodologie et illustration des premiers résultats pour le diagnostic des thromboses veineuse profondes». Journal d'Imagerie Médicale. 1: 193–197
- ↑ Dauzat M., Laroche J. P. (1983). «Lechotomographie des veines: proposition d'une méthodologie et illustration des premiers résultats pour le diagnostic des thromboses veineuse profondes». journal d'Imagerie Médicale. 1: 193-197
- ↑ Jewell R., Persson A.V. (199). «Use of triplex scanner in diagnosis of deep venous thrombosis». Arch. Surg. (124): 593-596
<ref> com nome "FOOTNOTEDauzat19915-6" definido em <references> não é utilizado no texto da página.

 French
French Deutsch
Deutsch