Тетраборан — Вікіпедія
| Тетраборан | |
|---|---|
 | |
| Систематична назва | Тетраборан(10) |
| Інші назви | арахно-B4H10 |
| Ідентифікатори | |
| Номер CAS | 18283-93-7 |
| ChEBI | 33592 |
| SMILES | [BH2]123[BH]45([BH2]6([BH]14([H]2)[H]6)[H]5)[H]3[1] |
| InChI | InChI=1S/B4H10/c5-1-3(5)2(7-3)4(1,3,6-1)8-2/h3-4H,1-2H2 |
| Номер Гмеліна | 49820 |
| Властивості | |
| Молекулярна формула | B4H10 |
| Молярна маса | 53,323 г/моль |
| Зовнішній вигляд | безбарвний газ |
| Густина | 2,180 г/л[2] |
| Тпл | -121 °C[2] |
| Ткип | 18 °C[2] |
| Якщо не зазначено інше, дані наведено для речовин у стандартному стані (за 25 °C, 100 кПа) | |
| Інструкція з використання шаблону | |
| Примітки картки | |
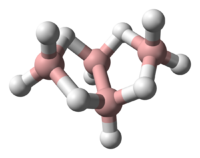
Те́трабора́н — неорганічна бінарна сполука ряду бороводнів складу B4H10.
Фізичні властивості[ред. | ред. код]
Тетраборан — токсичний безбарвний газ із неприємним запахом. Може легко займатися на повітрі. Зріджується за температури 18 °C, кристалізується за −121 °C.
Отримання[ред. | ред. код]
Вперше тетраборан було отримано за реакцією галогенпохідного диборану з металічним натрієм:
Іншими методами отримання тетроборану є піроліз диборану та кислотний гідроліз боридів лужних і лужноземельних металів:
- (вихід 14%)
Хімічні властивості[ред. | ред. код]
Тетраборан піддається гідролізу в гарячій воді:
Реакція з гідрогалогенідами дає заміщення атомів водню:
Тетраборан виявляє сильні кислотні властивості. З основами Льюїса (наприклад, з аміаком) утворює нестійкі комплекси:
Див. також[ред. | ред. код]
Примітки[ред. | ред. код]
Посилання[ред. | ред. код]
Джерела[ред. | ред. код]
- CRC Handbook of Chemistry and Physics / D. R. Lide. — 86th. — Boca Raton (FL) : CRC Press, 2005. — 2656 p. — ISBN 0-8493-0486-5. (англ.)
- Schubert D. M. Boron Hydrides, Heteroboranes, and their Metalla Derivatives // Kirk-Othmer Encyclopedia of Chemical Technology. — 4th. — New York : John Wiley & Sons, 2004. — Vol. 4. — P. 227—258. — ISBN 978-0-471-48517-9. — DOI: (англ.)
- Реми Г. Курс неорганической химии / А. В. Новоселова. — М. : ИИЛ, 1963. — Т. 1. — 922 с. (рос.)
| Це незавершена стаття про неорганічну сполуку. Ви можете допомогти проєкту, виправивши або дописавши її. |


 French
French Deutsch
Deutsch





![{\displaystyle \mathrm {B_{4}H_{10}+2NH_{3}\rightarrow [H_{2}B(NH_{3})_{2}]^{+}[B_{3}H_{8}]^{-}+H_{2}\!} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/20224ce5e9cf0b8ab66882fc3ff26305b200ac0a)
